上海和元生物技术(集团)股份有限公司品牌商
14 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
推荐产品
公司新闻/正文
项目文章(IF 12.9)| 周许辉/陶霞/孟怡辰研究揭示一种新型DCSTAMP拮抗剂通过调节RAP1B-RAC1介导的细胞骨架重塑来抑制破骨细胞前体融合
262 人阅读发布时间:2026-01-07 13:32
树突状细胞特异性跨膜蛋白(DCSTAMP)是一种关键的融合蛋白,在破骨细胞生成过程中调控细胞融合。尽管 DCSTAMP 具有治疗潜力,但目前尚未发现特异性的 DCSTAMP 抑制剂。
2025年12月22日,海军军医大学第二附属医院(上海长征医院)周许辉/陶霞/孟怡辰研究团队在Experimental & Molecular Medicine(IF=12.9)发表题为A novel DCSTAMP antagonist impedes preosteoclast fusion via modulation of RAP1B–RAC1-mediated cytoskeletal remodeling的研究成果。
该研究利用 AlphaFold 预测,及基于结构的虚拟筛选,鉴定出一种新型小分子 E8431,该分子选择性地靶向 DCSTAMP结构域。体外实验证实 E8431 能够抑制前破骨细胞融合,同时抑制骨吸收并刺激 PDGFBB 的分泌,从而促进成骨和血管生成过程。还阐明了一条此前未被发现的 DCSTAMP 信号通路,该通路涉及 DCSTAMP 与 RAP1B 的相互作用,并激活 RAP1-RAC1 信号通路诱导细胞骨架重组。此外,在小鼠模型中,E8431 给药可有效减轻卵巢切除术引起的骨丢失,且未观察到明显的毒性,这凸显了其作为骨质疏松症治疗药物的潜力。
·研究结果·
1. DCSTAMP结构域的破坏可减轻卵巢切除引起的骨丢失
DCSTAMP基因区域(±10 kb,hg19,chr11: 105342024-105378917)分析显示,该基因区域与eBMD 及DCSTAMP 表达存在显著关联。在该区域的 1202 个SNP中,有 89 个与 eBMD 显著相关,其中 rs2514663 是最显著的SNP位点(图1a)。证实了 DCSTAMP 表达升高与 eBMD 降低存在关联(图1a)。先前研究已证实DCSTAMP结构域,特别是其尾部区域(氨基酸398-470),在蛋白质功能和破骨细胞活性中发挥着关键作用(图1b)。为了研究DCSTAMP结构域完整性的重要性,构建了氨基酸398-470缺失的Dcstamp-tail敲除小鼠(Dcstamp-tail−/−)(图1c-e)。雌性Dcstamp-tail−/−小鼠的骨小梁表现出显著增生(图1f–j)。卵巢切除Dcstamp-tail−/−小鼠的骨量也得到了显著改善(图1f–j )。这些结果表明,DCSTAMP结构域的破坏会损害其功能,从而导致骨量增加。
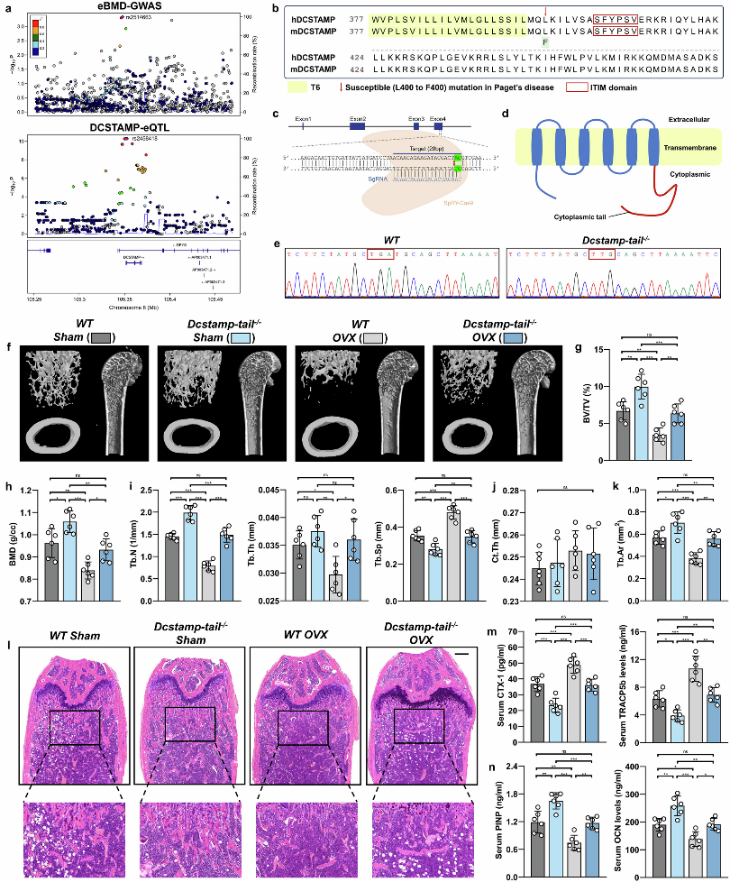
图1 DCSTAMP 结构域的破坏可导致小鼠骨量增加
2. Dcstamp-tail敲除抑制了破骨细胞生成,促进了成骨和血管生成
作者评估了DCSTAMP结构域缺失对破骨细胞、成骨细胞和内皮细胞的影响。TRAP染色显示,Dcstamp-tail−/−小鼠体内破骨细胞数量减少(图2a,b)。卵巢切除(OVX)也诱导Dcstamp-tail −/−小鼠中破骨细胞数量显著减少(图2a,b)。虽然 OVX 增强了 WT 细胞中成熟破骨细胞的形成,但 Dcstamp-tail −/− mBMM 在假手术和 OVX 条件下均表现出成熟破骨细胞形成受抑制(图2c、d、g、h)。骨形态学分析显示,OVX降低了WT小鼠的成骨细胞数量,但Dcstamp-tail −/−小鼠在假手术组和OVX组中均保持较高细胞数(图2e,i)。Dcstamp-tail敲除显著逆转了OVX引起的骨形成率/骨形成面积比(BFR/BS)和骨形成率(MAR)降低(图2f,j )。Dcstamp-tail −/−小鼠的内皮细胞数量增加(图2k-n)。Dcstamp-tail −/−小鼠骨髓中 PDGFBB 水平显著升高(图2o)。这些结果表明,Dcstamp-tail敲除抑制了破骨细胞生成和骨吸收,同时通过调节骨微环境间接增强骨形成和type H血管发育。
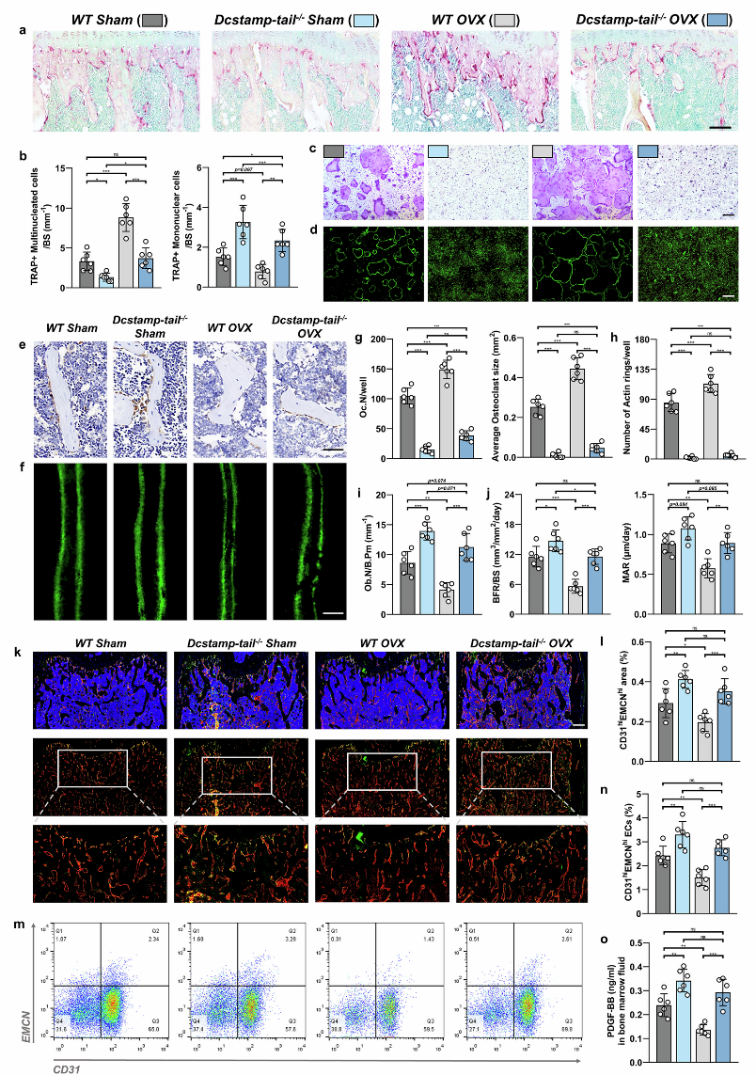
图2 Dcstamp tail−/−小鼠表现出骨吸收减少,同时骨骼和血管形成增强
3. 通过AlphaFold3 预测及虚拟筛选,发现了一种新型 DCSTAMP 拮抗剂E8431
利用AlphaFold3预测了DCSTAMP蛋白结构(图3a)。进一步分析显示,人和小鼠DCSTAMP序列显示其高度保守,并将结构域位置和潜在活性位点(红色高亮显示)进行了标注(图3g)。为了筛选潜在的DCSTAMP拮抗剂,基于Drugbank和Enamine化合物库进行了全面的分子对接虚拟筛选,最终筛选出5个化合物(图3i)。只有 Z2371498431在浓度高达 10 μM 时,对破骨细胞生成表现出显著抑制作用,且对小鼠骨髓巨噬细胞无细胞毒性(图3i –k)。因此,来自 Enamine 化合物库的 Z2371498431 被命名为 E8431,作为一种新型 DCSTAMP 拮抗剂进行进一步研究。
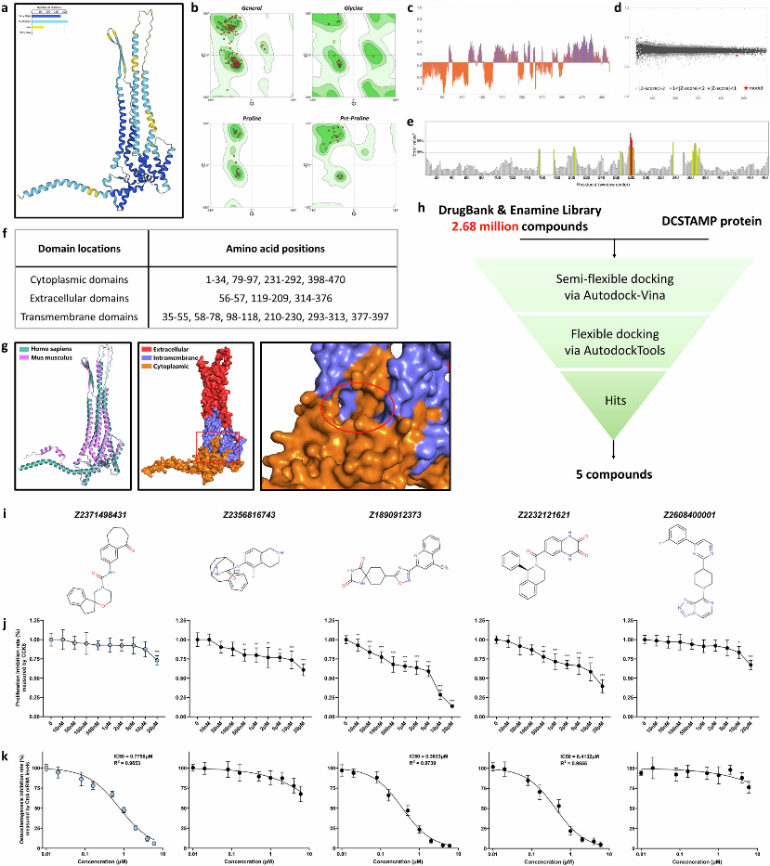
图3 DCSTAMP 拮抗剂的虚拟筛选和实验验证
4. E8431在体外抑制破骨细胞生成
柔性分子对接分析显示,E8431 与人源和鼠源 DCSTAMP 蛋白的结合能分别为-10.4 kcal/mol 和 -10.1 kcal/mol(图4a、b)。此外,DCSTAMP尾部结构域的缺失消除了 E8431 与DCSTAMP 的分子相互作用(图4c)。利用小鼠骨髓单核细胞(mBMMs)进行体外实验,评估E8431对破骨细胞的影响。TRAP染色结果显示,E8431呈剂量依赖性地抑制成熟破骨细胞生成,其中2 μM E8431的抑制效果最佳(图4d,h)。E8431减少了功能性破骨细胞的数量,表现为肌动蛋白环减少(图4e,i)。破骨细胞融合实验表明,破骨细胞前体膜融合率显著降低;E8431处理后破骨细胞的骨吸收面积减少(图4f,g,j,k)。成熟破骨细胞特异性标志物(Oscar和Ctsk)在所有浓度下均呈显著下调表达(图4l)。这些研究结果表明,E8431通过与DCSTAMP蛋白结合抑制破骨细胞融合和吸收。
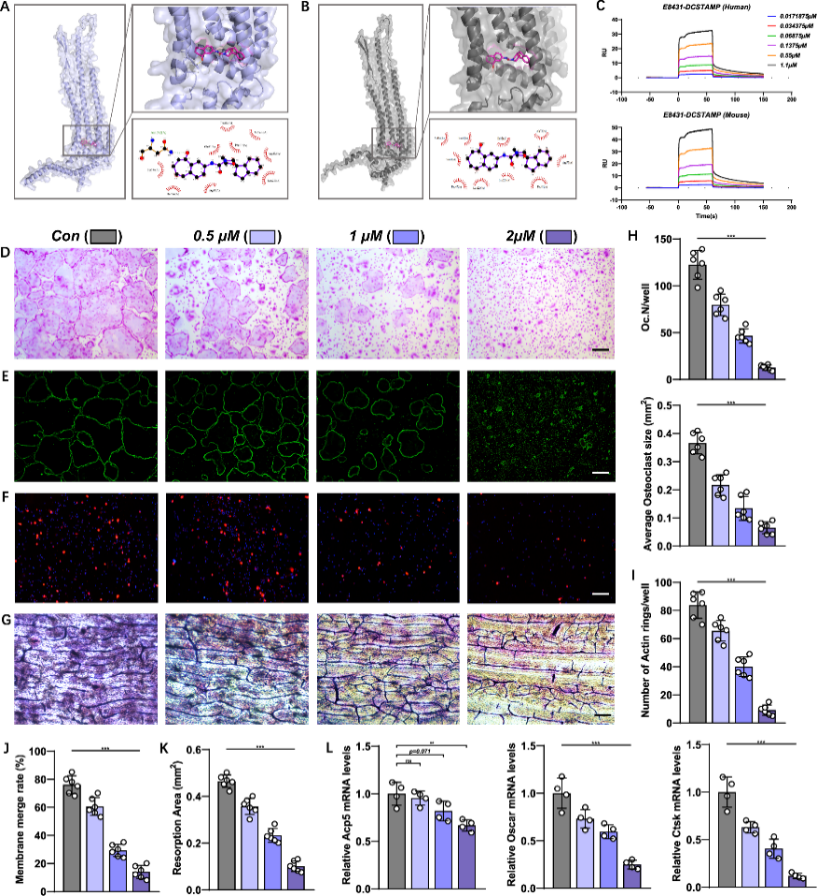
图4 DCSTAMP 拮抗剂在体外抑制破骨细胞前体融合和骨吸收
5.E8431在体外促进血管生成
为了探究E8431对血管生成的影响,建立了一个包含间充质干细胞/小鼠原代内皮祖细胞(mEPCs)和破骨细胞的共培养系统(图5a)。E8431处理后PDGFBB表达显著升高(图5b)。E8431处理显著增强了mEPC迁移能力(图5c-f),促进了mEPC管状结构形成(图5g,h)。此外,在共培养系统中引入 PDGFBB中和抗体则完全消除了 E8431 在体外介导的促血管生成作用(图5a-h)。
利用Transwell小室建立了共培养系统,将mBMMs和mBMSCs分别接种于上室和下室(图5i)。共培养组的ALP活性显著增强,E8431处理显著增强了这种效应(图5j,l),且显著提高了OCN表达(图5k,m)。成骨标志基因,包括Runx2、ALP和Bglap,在E8431处理组中也显著上调表达(图5n)。此外,将 PDGFBB 中和抗体加入共培养体系中,完全消除了 E8431 在体外赋予的促骨形成作用(图5i-n)。这些研究结果表明,E8431 通过保存破骨细胞前体并随后激活 PDGFBB 介导的 PI3K–FAK 信号转导来增强 hBMSC 成骨作用。
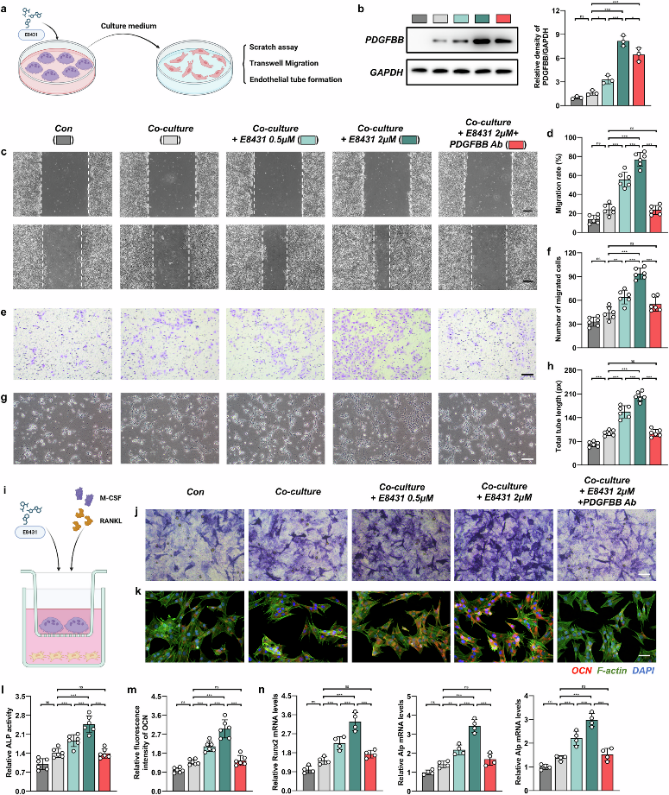
图5 DCSTAMP 拮抗剂通过抑制PDGFBB 分泌来增强成骨和血管生成
6. E8431抑制卵巢切除术引起的骨骼退化
卵巢切除小鼠经E8431治疗6周后,完全逆转了OVX引起的骨丢失(图6a-c)。E8431治疗使OVX降低的骨小梁面积恢复至与假手术组相当的水平(图6d, e)。E8431使骨转换相关的血清标志物(包括CTX-1和PINP)表达恢复正常,表明其对成骨和破骨细胞生成具有双重调节作用(图6f, g)。E8431减少了TRAP阳性多核细胞(成熟破骨细胞),同时增加了TRAP阳性单核细胞(前破骨细胞)(图6h,i)。E8431治疗后OCN阳性细胞数显著增加(图6j,k)。E8431恢复了OVX抑制的骨形成率(图6l,m)。E8431治疗后OVX诱导的H型内皮细胞减少得到了恢复(图6n-p,r)。E8431 治疗后小鼠骨髓 PDGFBB 表达显著升高(图6q)。这些结果表明 E8431 是一种治疗骨质疏松症的潜在药物。
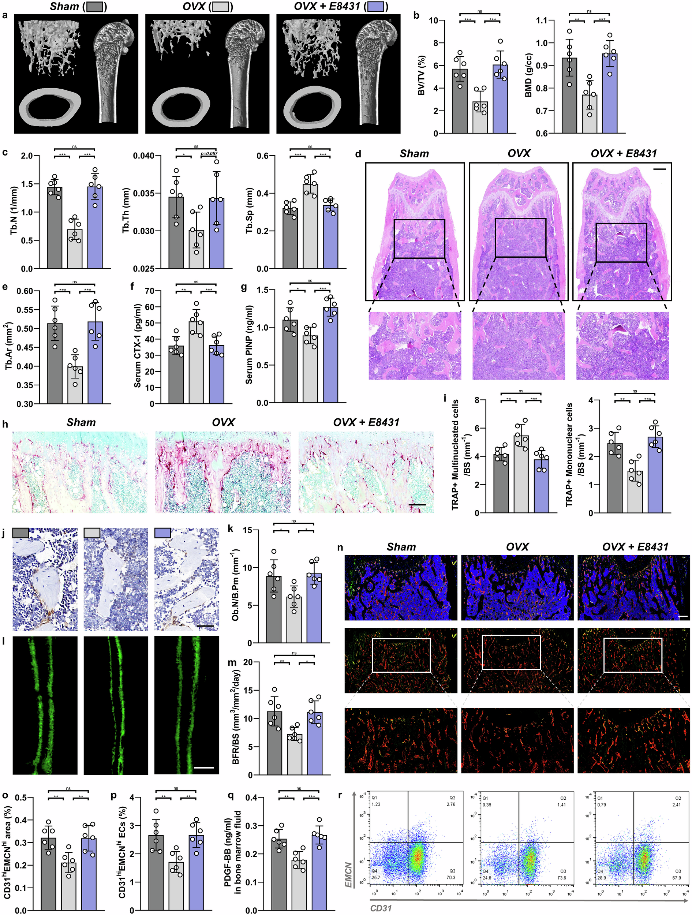
图6 DCSTAMP 拮抗剂可减轻小鼠因雌激素缺乏引起的骨质流失
7. DCSTAMP 功能缺失会导致破骨细胞生成过程中 RAP1–RAC1 信号通路的抑制
进一步研究了E8431的分子机制。从WT、Dcstamp-tail −/−和E843+WT小鼠中分离mBMMs,进行RNA测序。Dcstamp-tail −/−组和 E8431 组中关键破骨细胞基因均表现出下调,包括 Ctsk、Dcstamp、Car2、Mmp9、Atp6v1b2、Oscar、Mmp14 和Ocstamp等(图7b)。在 Dcstamp-tail −/−组中,重叠的下调基因约占所有下调基因的 50%,而在 E8431 处理组中,这一比例约为三分之二,表明存在显著的机制趋同性(图7c)。相比之下,上调基因在 Dcstamp-tail −/−组和 E8431 处理组之间的一致性较低(图7d)。
随后对Dcstamp-tail −/−组和E8431处理组之间共同下调基因进行了富集分析。GO分析显示,这些基因在骨重塑、骨吸收、GTP酶介导的信号转导、肌动蛋白丝相关过程中显著富集(图7e)。KEGG通路分析发现,Rap1信号通路显著富集(图7f)。GSEA分析也表明Rap1信号通路显著下调(图7g)。WT组中RAP1、RAC1及Syk和Src的磷酸化水平显著升高;而Dcstamp-tail敲除和E8431处理均显著减弱了这些效应(图7h,i)。利用 Rap1 激动剂 8-CPT-2′-O-Me-cAMP 进行挽救实验,部分挽救了Dcstamp-tail敲除和 E8431 处理下观察到的成熟破骨细胞形成受损(图7j–n)。这些发现证实 RAP1–RAC1 信号通路及其相关的细胞骨架重塑是 DCSTAMP 介导信号通路的关键下游效应因子。
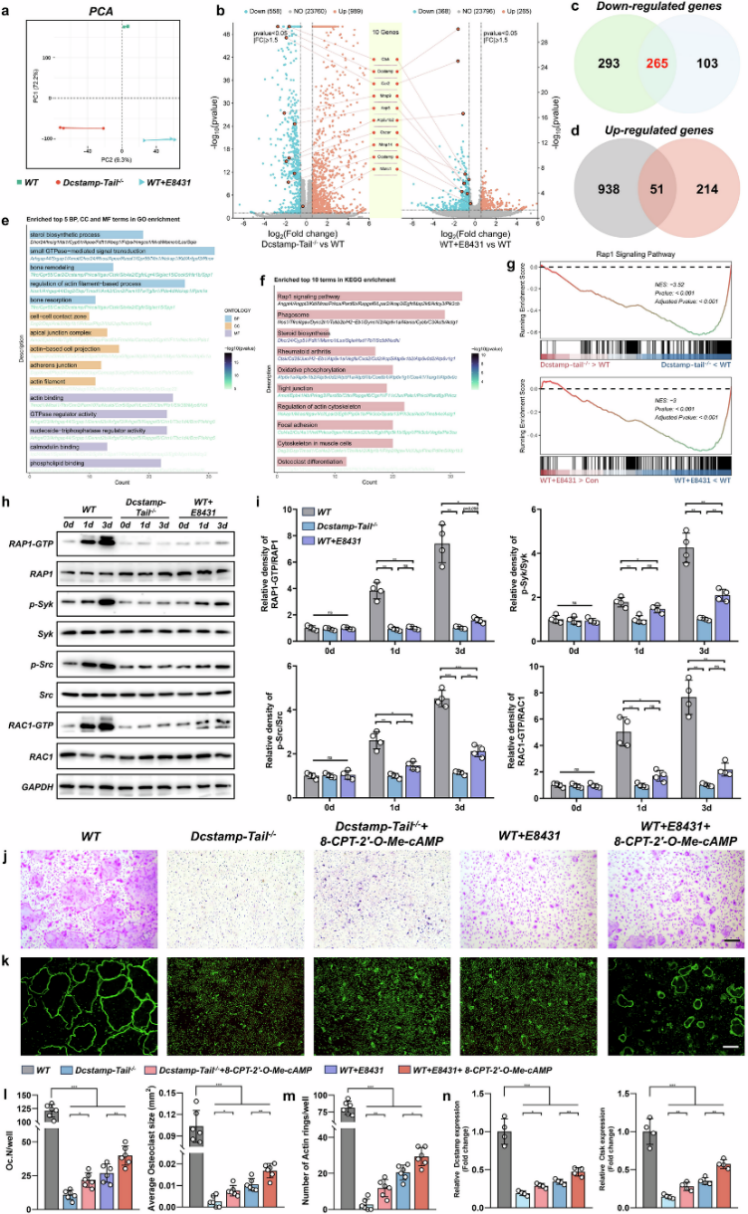
图7 干扰 DCSTAMP 功能会导致破骨细胞生成过程中 RAP1–RAC1 信号通路的抑制
8. DCSTAMP-tail敲除或E8431处理可有效抑制DCSTAMP与RAP1B的结合
为了阐明 DCSTAMP 调控 RAP1–RAC1的机制,使用 DCSTAMP 抗体在WT和 Dcstamp-tail −/−细胞裂解液中进行了Co-IP实验(图8a)。值得注意的是,在WT中检测到了 RAP1B,但在 Dcstamp-tail −/−中未检测到,表明 RAP1B 可能直接调控 RAP1–RAC1 信号通路(图8a,b)。尽管RAP1A与DCSTAMP或RAP1B均无相互作用,但RAP1B在野生型条件下与DCSTAMP表现出强烈的结合,而Dcstamp-tail 敲除和E8431处理均显著降低了这种结合(图8c)。使用RAP1A抗体进行的反向共免疫沉淀实验证实了RAP1A与DCSTAMP和RAP1B均无相互作用,而RAP1B免疫共沉淀验证了其与DCSTAMP的直接相互作用(图8d,e)。此外,与DCSTAMP结合的RAP1表现出显著激活,这种激活被Dcstamp-tail敲除完全消除,并被E8431处理显著降低(图8f)。分子对接分析揭示了 RAP1B 与 DCSTAMP结构域的相互作用(图8g)。预测 E8431 会占据 DCSTAMP 的活性位点,该位点位于这两个蛋白的界面处,并可能破坏它们的相互作用(图8h)。综上所述,这些结果表明 DCSTAMP 通过直接结合RAP1B 来激活下游 RAP1-RAC1 信号通路,而 DCSTAMP结构域的缺失或 E8431 处理均可有效抑制这一过程(图8i)。
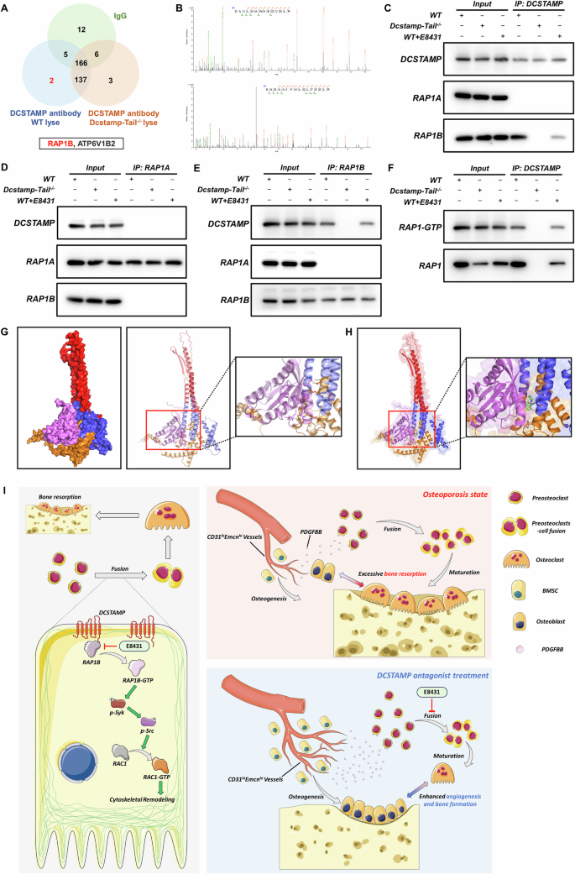
图8 DCSTAMP 拮抗剂阻碍 DCSTAMP 与 RAP1B的相互作用,从而抑制细胞骨架重塑和破骨细胞生成
和元助力
和元生物有幸为研究者提供转录组测序(RNA seq)服务,以实际行动助力基础科学研究!

和元多组学服务
和元生物提供多组学服务(如转录组、Astral蛋白组、代谢组、微生物组、Cut&Tag等)和单细胞及空间转录组服务(如10x Genomics GEM-X单细胞转录组(V4.0)、10x Genomics单细胞转录组(V3.1)、10x单细胞转录组及TCR/BCR、墨卓单细胞转录组、DNBelab C-TaiM4单细胞转录组、CytAssist空间转录组、HD空间转录组、Stereo-seq 空间转录组等),致力于为广大生命科学家、医学工作者提供基于多组学的科研及临床应用解决方案。累计协助客户在Advanced Science、Journal of Nanobiotechnology、Advanced Functional Materials、ACS Nano、Nature Aging、Neuron等期刊发表SCI论文,并推出了广受好评的生信分析云平台【】,助您高效实现个性化数据挖掘!

更多活动详情可长按或扫描上方二维码,填写表单,我们将尽快安排专人与您联系!
和元生物:15800353038
和元生物技术(上海)股份有限公司(股票代码:688238)作为一家在科创板上市的高新技术企业,自2013年成立以来,始终深耕细胞和基因治疗核心领域,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务,可提供①组学服务:常规转录组、单细胞转录组、基因组、代谢组及蛋白组等。②载体构建和病毒包装:质粒、siRNA、腺相关病毒(AAV)、腺病毒(ADV)、慢病毒(LVV)、逆转录病毒(RV)、单纯疱疹病毒(HSV)等病毒载体生产服务,提供R&D、实验室级别、GMP级别,满足研发、小动物、大动物NHP到临床的不同研究阶段的使用需求。③细胞实验服务:过表达、干扰稳定株构建,单克隆细胞株构建服务及细胞功能学、药效学实验服务。④动物实验及机制研究:神经、代谢、肿瘤动物模型、药效药代、病理切片及蛋白、核酸检测服务。⑤特色项目服务:CRISPR文库筛选服务,外泌体整体研究服务,AAV衣壳筛选服务、听力研究整体项目服务,满足客户定制化或一站式项目服务,助力基础科学研究,促进基础研究到临床转化应用,推动细胞和基因治疗行业发展。