上海和元生物技术(集团)股份有限公司品牌商
14 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
推荐产品
公司新闻/正文
Mol Cancer | 徐瑞华/王峰/赵齐教授团队绘制食管小细胞癌单细胞转录组图谱
671 人阅读发布时间:2025-09-17 16:27
食管癌中仅占0.8%-2.4%的食管小细胞癌(SCCE),因侵袭性强、预后极差,长期被称为“难治性神经内分泌恶性肿瘤”。为了更好地理解SCCE的分子模式,研究人员首次对SCCE进行了综合分析,揭示了关键的基因组改变,并提供了其发病机制的见解。
2025年5月15日,中山大学肿瘤防治中心徐瑞华、王峰、赵齐教授团队在“Molecular Cancer(IF=27.7)”发表了题为“Dissecting small cell carcinoma of the esophagus ecosystem by single-cell transcriptomic analysis”的研究成果。作为国内最早开展 SCCE 研究的团队(2018 年首次解析 SCCE 基因组特征),徐瑞华/王峰/赵齐团队此次通过单细胞技术实现 “从宏观到微观” 的跨越。通过单细胞转录组结合T细胞受体(TCR)测序,对SCCE患者的肿瘤样本进行分析,以阐明SCCE的完整肿瘤微环境(TME),解析上皮细胞的异质性,并探讨抗血管生成治疗在SCCE患者中的潜在应用。系统阐释了 SCCE 的免疫抑制与血管生成机制,更通过生态类型与元程序分析,为该罕见癌种的精准分型和个体化治疗奠定了基础。
研究结果
01 食管小细胞癌的高分辨率单细胞图谱
为了阐明 SCCE 和 ESCC 之间的细胞异质性,对从 SYSUCC 收集的10个SCCE 患者的肿瘤样本进行 scRNA-seq 分析,并与21 个(包含正常食管粘膜、ESCC 和配对癌旁组织 NAT)已发表scRNA-seq 数据进行整合分析,另对 7 个样本进行了单细胞 V(D)J 分析(图1A、D)。经过质量过滤,获得了 197,858 个高质量单细胞,并将其注释为10 个细胞簇,包括 B 细胞(MS4A1、CD19)、树突状细胞 (CD1C、CLEC9A)、内皮细胞(PECAM1、VWF)、上皮细胞(EPCAM、KRT18)、成纤维细胞(COL1A1、DCN)、肥大细胞(TPSAB1、CPA3)、髓样细胞(CD14、S100A8)、中性粒细胞(CSF3R、IL1R2)、浆细胞(MZB1、JCHAIN)和 T/NK 细胞(CD3D、CD3E、NKG7、FCGR3A)(图 1B)。为了更好地了解 TME 的异质性,分析了不同组织亚型之间的细胞组成,发现上皮细胞主要富集在正常上皮粘膜中。SCCE 和 ESCC相比,上皮细胞、髓系细胞和中性粒细胞主要分布在 SCCE 中;而 B 细胞、T 细胞、肥大细胞和成纤维细胞在 ESCC 中富集(图1C-D)。
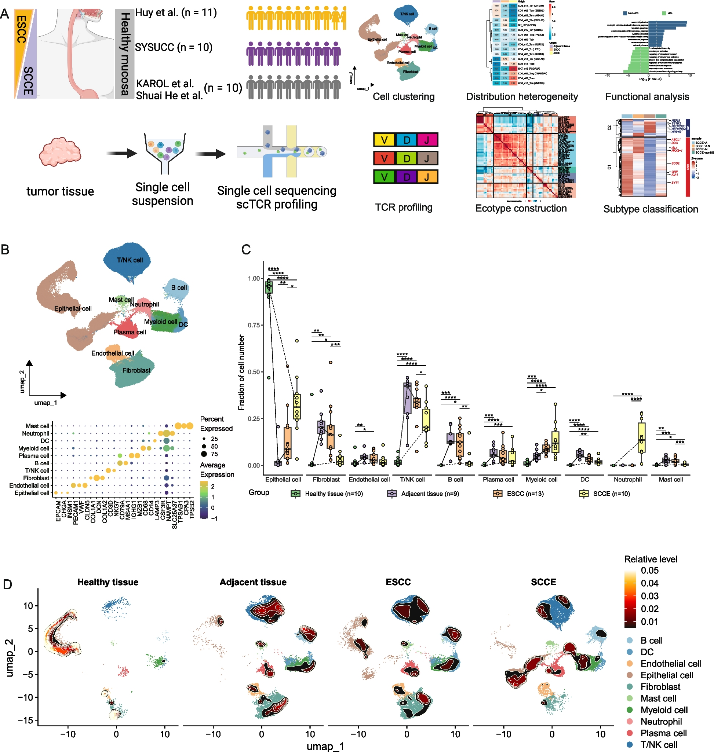
图1 食管比较队列中免疫、基质和上皮细胞的单细胞图谱
02 食管小细胞癌中抑制性肿瘤微环境的形成
T 细胞在抗肿瘤免疫中起着至关重要的作用。在 41,906 个细胞上构建了 T/NK 细胞的综合图谱,分为四大簇,包括 CD4T、CD8T、NK、NKT(图 2A)。在CD8+T细胞中鉴定了 8 个亚簇,包括Tem细胞 (c08、c10),Teff细胞 (c11、c12),Tstr细胞 (c09),Trm细胞 (c13),Tex细胞 (c14),Tpro细胞 (c15)(图 2A-C)。为了探索不同CD8+T细胞簇之间的分化关系,进行拟时序分析并确定了两种不同的分化轨迹(图 2D)。它们都从 CD8_c08_Tem(ANXA1) 开始,然后是 CD8_c09_Tstr、 CD8_c10_Tem (KLRC1) 和 CD8_c13_Trm (ZNF683) 分支。一个分支变为耗竭状态并在 CD8_c14_Tex(CXCL13) 终止,而另一个分支持续细胞毒性并分化为效应 T 细胞,如CD8_c12_Teff (GZMK) 和 CD8_c11_Teff (CRTAM)。正如预期,两种食管癌ESCC 和 SCCE,都与具有耗竭 T 细胞状态的分支1对齐,而带有分支 2 的 ESCC 的 NAT 在进化过程中维持细胞毒性(图 2E)。TCR-seq 分析验证了 SCCE 的进化轨迹。CD8_CXCL13 T 细胞在 SCCE 中具有高比例的克隆扩增。在克隆重叠分析中,CD8_Trm_ZNF683与 CD8_c14_Tex (CXCL13) 的克隆重叠高于 CD8_c12_Teff (GZMK),这表明 SCCE 中的进化谱系已穷竭。
在 CD4+T 细胞中鉴定了 7个亚簇,包括Tn细胞(c01)、Tcm细胞 (c02)、Tem细胞 (c03)、Tfh细胞 (c04)、Treg(c05-06)、Tpro细胞 (c07)(图 2A)。接下来将所有 Treg细胞重聚类为 5 个亚型,并探索进化轨迹(图2H-J)。Treg_c1高度表达的幼稚基因 (如 LEF1、CCR7) 位于两个进化分支的起点。Treg_c4高表达HLA 分子,被认为是过渡态,位于轨迹的中心。然后一个分支转向 Treg_c2,它高度表达 FOXP1,FOXP1 是 Treg 细胞静止和稳态的关键调节因子。另一个分支进入Treg_c5,其特征是FOXP3、CTLA4 和共刺激分子的高表达并被激活。有趣的是,发现 Treg_c4_transitional和Treg_c5_activated在SCCE 中高度富集,表明 Treg 对 SCCE 中抑制性 TME 的形成有很大贡献(图 2K-L)。综上所述,两种食管癌均表现出具有不同特征的抑制性 TME。ESCC表现出了免疫分子检查点因子高表达的耗竭 CD8 T 细胞的显著富集,而 SCCE 富集了更多活化的 Treg 细胞。
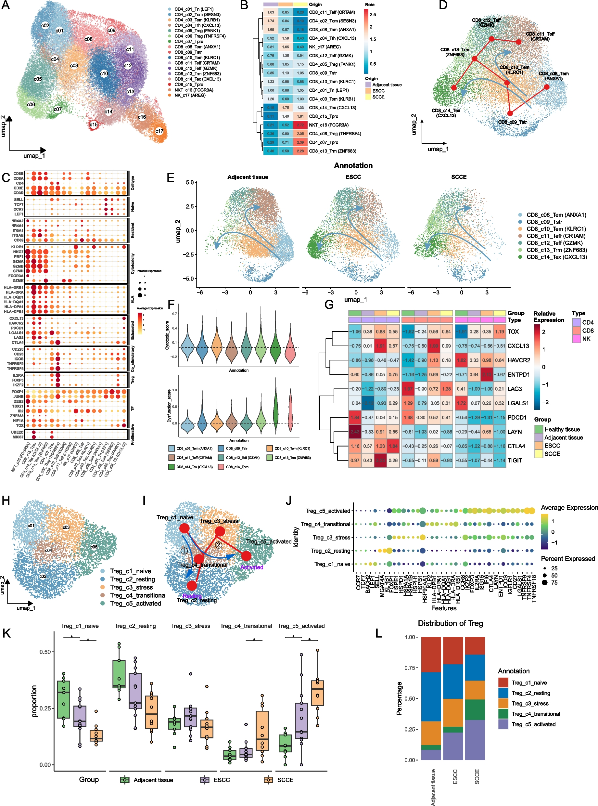
图2食管比较队列中不同组织的 T 细胞特征分析
03 食管小细胞癌中高度分化的B细胞和浆细胞
为了进一步剖析 SCCE 中 B 细胞,将所有 B 细胞分为9个细胞亚簇(图 3A-B)。鉴定了以 TCL1A 表达为特征的幼稚 B 细胞 (Bn,c1),TCL1A 主要富集在 ESCC 的 NAT 中;表达 HSPA6 的应激相关 B 细胞 (Bstr,c4);以 RGS13 、 SUGCT 、 MME 为特征的Bgem细胞 (c8)。CD45RA+CD27-B细胞被视为早期记忆 B 细胞 (Bem,c2/c5/c6/c9);而 CD45RA+CD27 +B 的晚期记忆 B 细胞 (Bm,c3/c7),表现出较高的阳性免疫调节和抗原呈递评分(图3C-D)。有趣的是,SCCE 和 ESCC 之间 B 细胞的组成差异很大。晚期记忆 B 细胞在 SCCE 中表现出高度富集,而早期记忆 B 细胞在 NAT 和 ESCC 中表现出高度富集。
在浆细胞中也发现了相同的分布趋势,浆细胞根据其分泌抗体分为六个亚簇(图 D3E-F)。通过 Cytotrace 推断细胞分化状态,表明 IgD/M+PCs 分化最少,其次是 lgA+PCs 和 IgG+PCs;IgG1+PCs 细胞的得分最低,表明其分化状态最高(图 D)。在正常的胃肠道和呼吸组织中,lgA 抗体有助于维持粘膜免疫力。然而在肿瘤发生过程中,lg 类转换为 IgG 主要发生在肿瘤区域,启动抗体介导的免疫反应。为了进一步量化 lg 转换过程,计算了不同组织之间的 lgG/IgA 评分,发现 SCCE 中具有最高得分,表明 SCCE 中 B 细胞介导的免疫反应更活跃(图3H)。
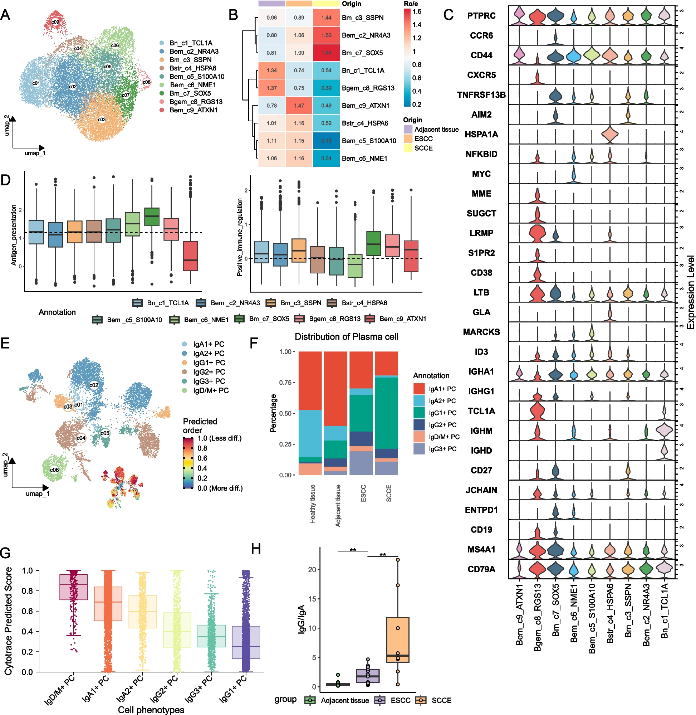
图3 食管比较队列中不同组织的 B 细胞和浆细胞特征分析
04 食管小细胞癌中血管诱导型生态位的形成
髓样细胞主要分布在 SCCE 中。另发现了 5 簇具有不同功能的巨噬细胞(图 4A)。其中Macro_c01_FCN1 和 Macro_c03_HSPH1 在 SCCE 中显示出更多的富集,具有高血管生成相关标志物和特征,而 Macro_c04_LYVE1 在 ESCC 中富集,具有高吞噬作用特征(图4B)。接下来,探讨了两种不同组织来源的巨噬细胞之间的功能状态,发现 SCCE 巨噬细胞高度表达 S100A8/9/12、FCN1、VCAN 和 IL1B,这些基因与巨噬细胞的血管生成表型和侵袭特性相关。然而,ESCC 中的巨噬细胞上调了 HLA 分子、CXCL1/3、C1Q 和 APOE,表明 ESCC 中的巨噬细胞可能在抗原呈递和 T 细胞募集中发挥重要作用(图4C)。通路分析还显示 SCCE 中中性粒细胞活化和 NFκB 信号通路的显着富集,而补体激活和脂质代谢相关通路在 ESCC 中富集。通过计算组织驻留评分进一步探索了来自两个组织谱系的巨噬细胞的潜在来源,Macro_c04_LYVE1 在 3 种巨噬细胞中排名最高,表明 ESCC 的巨噬细胞可能来源于组织驻留。
对于非免疫细胞,将内皮细胞分解为两大簇,包括血管内皮细胞和淋巴内皮细胞。内皮细胞根据其表标志物进一步聚集成 7 个亚簇,其中 Endo_c2_CACNA1C 和 Endo_c3_ESM1 细胞主要富集在 SCCE 中(图4D-E)。此外,Endo_c3_ESM1 具有Tip 样特征(图 4F)。 进一步,对富含SCCE和ESCC的内皮簇进行了差异表达分析。Endo_c2_CACNA1C 和 Endo_c3_ESM1(主要富集在SCCE中)表达高水平的 PGF、CCL2、CCL14、CXCL1、MMP1、AKR1C等,这些基因参与血管生成、炎症、基质重塑和代谢重组。相比之下,Endo_c4_ FGF7(主要富集在ESCC中)高度表达 PIEZO2。表明 SCCE 中的内皮细胞可能对 TME 的形成做出更多贡献(图4G)。
细胞通讯分析表明,巨噬细胞亚簇和内皮细胞之间的特定相互作用主要与血管生成信号有关。其中Macro_c01_FCN1巨噬细胞通过 VEGF-VEGFR 相互作用与 Endo_c3_ESM1内皮细胞有很强的串扰(图 4H-I)。发现经典血管生成受体 KDR、ITGB1 在 Endo_c3_ESM1中表达水平最高,包括 KDR-VEGFA、FGF1-FGFR1、IGF2-IGF2R 在内的多个配体-受体对介导 Macro_c01-03 和 Endo_c2-3 之间的串扰。正如最近报道的那样,TME 中巨噬细胞和内皮细胞的串扰在血管生成中起重要作用。
对于基质细胞,在SCCE中发现了两簇高表达RGS5 的周细胞,并显著上调了黏着斑和细胞连接通路(图4J-K)。此外,发现Pericyte_c07_EGFL6与Endo_c3_ESM1呈正相关,Pericyte_c07_EGFL6周细胞通过 PGF-VEGFR1 和 PLAU-PLAUR 信号通路与Endo_c3_ESM1内皮细胞相互作用(图4 L-M)。为了概括研究发现,在SCCE 中形成了由 FCN1 + 巨噬细胞、ESM1 + 内皮细胞和 RGS5 + 周细胞组成的诱导血管生成的生态位。免疫荧光揭示了新生血管形成场景,伴有血管诱导的巨噬细胞浸润,为 SCCE 治疗提供了一个有前途的新靶点(图4N)。
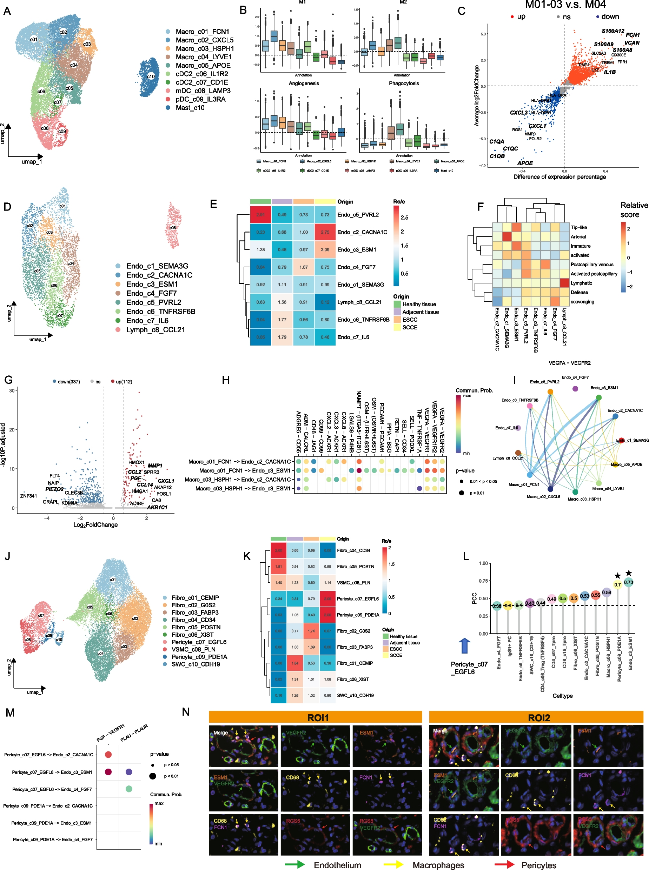
图4 食管比较队列中不同组织的髓系和基质细胞特征分析
05 肿瘤微环境细胞的组成及生态类型
接下来探讨了 66 个 TME 细胞亚群之间的相似性和功能关系。髓系细胞和淋巴细胞结合形成一个主要分支,而基质细胞形成另一个分支。值得注意的是,中性粒细胞主要富集在 SCCE 中,与 T、B 淋巴细胞的相似性高于骨髓细胞(图 5A)。为了更好地了解这些细胞亚群如何在 TME 中协调在一起形成有凝聚力的生态型,对不同细胞亚群之间的spearman 相关系数进行了无监督聚类分析,确定了五种具有不同细胞组成和组织分布的生态型 (EC1-EC5)(图 5B)。EC1 富集于 SCCE,主要包含肿瘤相关的中性粒细胞和 T 细胞簇,包括所有中性粒细胞亚群、驻留 T 细胞 (CD8_c13_Trm)、耗竭 T 细胞 (CD8_c14_Tex)、增殖 T 细胞和 NKT。中性粒细胞脱颗粒和细胞趋化途径的上调表明以 EC1 为主的患者表现出中性粒细胞处于活化状态。EC5 分布在 ESCC 和 SCCE 中,而 EC3、4 分散在不同的组织谱系中(图 5B-C)。此外,EC1 与更好的临床获益呈正相关。在 SCCE-A 亚型中,具有高 EC1 特征的患者也具有更好的总生存期(图 5D-G)。总体而言,基于单细胞的生态型提供了对 SCCE 中 TME 和预测生物标志物的全新视角。
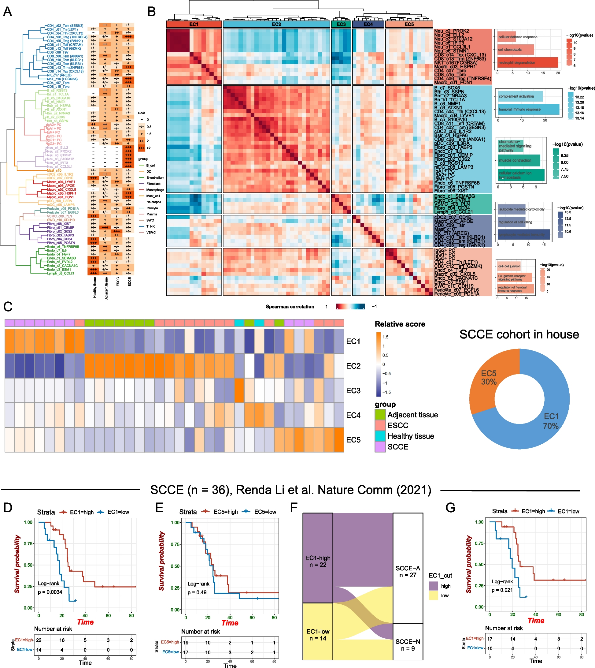
图5 不同组织来源的肿瘤微环境成分生态类型及其临床相关性
06 解析食管小细胞癌恶性细胞的异质性
考虑到 SCCE 和 SCLC 的细胞形态学和转录相似性,在 SCCE 患者中检测了几种 NE TFs 的表达,包括 ASCL1、NEUROD1/2、YAP1、POU2F3 和两个新定义的标志物 HNF4G、FOXA3,(图6A)。在SCCE 队列中,SCCE-nonNE 均匀分布在每位患者中,而 SCCE-N 仅集中在患者 09 和 SCCE-A 中;在这10个SCCE患者中表现出巨大的异质性(图 6C)。为了推断 SCCE 的进化轨迹,应用 cytotrace 来分析,发现 SCCE-A.N 显示出最高的干性,而 SCCE-N 表现出高度的分化。
考虑到 NE 肿瘤的所有分类方法都是基于 TF 转录的,因此在单细胞水平上开发了一种新的分类框架。确定了每位患者优先表达的 30 个基因的基因模块,随后将 120 个基因模块聚合到 8 个MP中(图 6D-E)。MP7 在细胞周期和增殖标志物 (即 G2M_checkpoint) 中独特富集。MP5 主要富集于神经内分泌相关通路 (即 androgen_response 和 estrogen_response_late)。MP1 和 MP4 均表现出应激相关特征 (即 UV_response),而 MP4 还富含细胞凋亡和缺氧途径。MP2 在 KRAS 信号转导和上皮-间充质转化途径中表现出高度富集。MP6 和 MP8 在干扰素反应通路中富集,而 MP8 在 p53 和雌激素反应通路中也显示出高度富集(图 6D)。为了进一步探索不同 MP 之间的关系,进行了相关性分析以推断其相互作用。MP1 与 MP2/3/4显著共存,表明所有这些 MPs 都具有与压力相关的特征;MP5 与 MP6 高度排斥,表明神经内分泌表型可能与炎症和细胞凋亡途径呈负相关,表现出恶性表型(图 6F)。此外发现 MP5 仅分布在 Patient09 和 SCCE-N 亚型中,与 MP5 的神经内分泌表型一致;另发现 MP5 与 SCCE 患者较短的 OS 显著相关(图6G)。
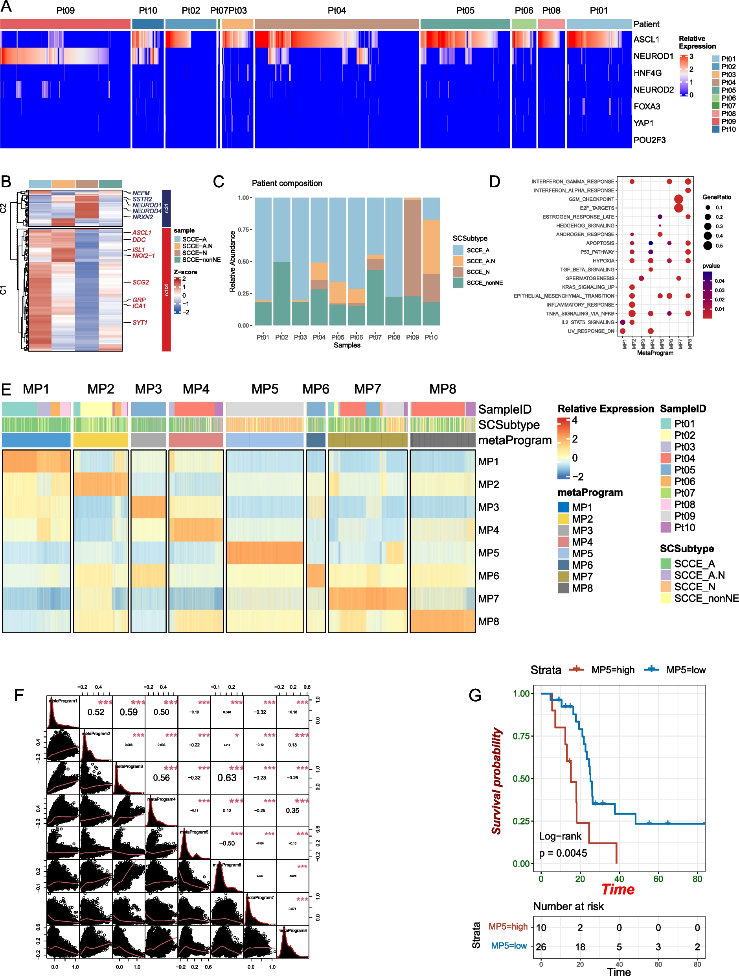
图6基于经典转录因子表达和元程序定义的食管小细胞癌异质性
和元服务
和元生物提供多组学服务(如全外显子测序、转录组、Astral蛋白组、非靶向代谢组、非靶向脂质组、靶向代谢组、16s/ITS/18s扩增子测序、宏基因组、Cut&Tag、MeRIP (m6A)-seq、全基因组甲基化测序、简化甲基化测序等)和单细胞及空间转录组服务(如10x单细胞转录组、10x单细胞转录组及TCR/BCR、墨卓单细胞转录组、10x CytAssist空间转录组、10x HD空间转录组、Stereo-seq 空间转录组等),致力于为广大生命科学家、医学工作者提供基于多组学的科研及临床应用解决方案。
业务咨询:15800353038