上海和元生物技术(集团)股份有限公司品牌商
14 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
推荐产品
公司新闻/正文
Nature neuroscience | 解析人体脊髓胚胎发育之谜
237 人阅读发布时间:2025-09-09 13:08
2023年4月24日,国际合作组织“人类发育细胞图谱(Human Developmental Cell Atlas)”的核心团队、来自瑞典卡罗林斯卡医学院的助理教授李霄飞博士与Erik Sundström教授团队在Nature Neuroscience(IF 25)上发表了文章Profiling spatiotemporal gene expression of the developing human spinal cord and implications for ependymoma origin,利用scRNA-seq、空间转录组(10x Visium)与原位测序(in situ sequencing)三大方法,描绘了人体脊髓胚胎发育的细胞图谱,并且与小鼠的胚胎发育进行对比从而解析了人体脊髓发育之谜。
1 人类脊髓发育的时空图谱
为了研究发育中的人类脊髓的分子特征,在 W5-12 期获得了 16 条人类产前脊髓,通过scRNA-seq、ST和HybISS建立了人类脊髓发育时空图谱(图1a)。scRNA-seq 鉴定到了159,350 个高质量细胞,发现了 16 个主要细胞群,包括 NPCs、中间神经元祖细胞(INPs)、兴奋性神经元(ExNs)、抑制性神经元(IbNs)、胆碱能神经元(ChNs)、星形胶质细胞(ASCs)、室管膜细胞(EPCs)、少突胶质细胞前体细胞(OPCs)和少突胶质细胞(OLs)(图 1b),这些是本研究主要关注的细胞类型。还有一些其他的细胞类型,如许旺细胞(SWCs)、周细胞(PCs)、内皮细胞(ENs)、VCLPs和免疫细胞(Immune)(如小胶质细胞)也在这一发育阶段衍生出来(图 1b)。为了确定空间基因表达和细胞类型定位,分析了代表性年龄段(W5、W8、W9 和 W12)出生前的rostral–caudal (RC) 的空间转录组数据,沿 RC 和 DV 轴形成了 12 种主要细胞类型(图 1d)。在W5时,人脊髓中主要是NPC;从 W8 开始,神经元和所有神经胶质细胞类型都出现了(图 1d)。将 HybISS与 scRNA-seq数据整合,证实了 ST 所揭示的结果(图 1e-f)。
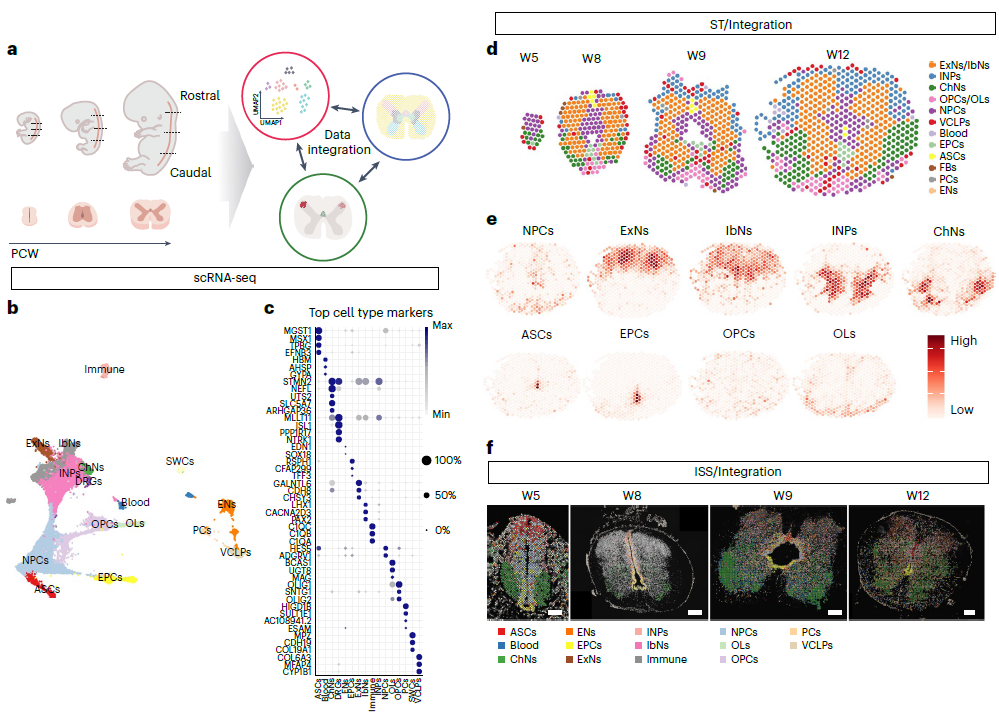
图1发育中的人类脊髓时空图谱
2 发育中脊髓的多种神经细胞
HybISS证实了 ST 结果:神经元(NPCs)(ASCL1+SOX2+)是 W5 期的主要细胞群,具有高度增殖性(MKI67+TOP2A+),但从 W8 期开始就局限于ventricular zone(图 2a);ExNs(CACN2D1+)、IbNs(SCGZ+ 或 NRXN3+)和 ChNs(ISL1+ 和/或 SLC5A7+)在内的神经元早在 W5 时就出现,在 W8 时广泛分布于整个灰质(即中间区)(图 2a)。IHC结果表明,在W5时脊髓背侧和腹侧区域分别出现了ASCs(MSX1+GFAP+)和EPCs(RFX4+FOXJ1+),这与HybISS结果一致(图2b,c)。但是,直到W8时才观察到了OPC细胞(PDGFRa+OLIG2+)(图 2d)。这些数据表明,在发育中的人类脊髓中,NPCs 早在 W5 时就已趋向于神经胶质化。为了进一步描述细胞类型的亚群状态,分别分析了主要的神经细胞类型,以揭示其多样性(图 2e)。
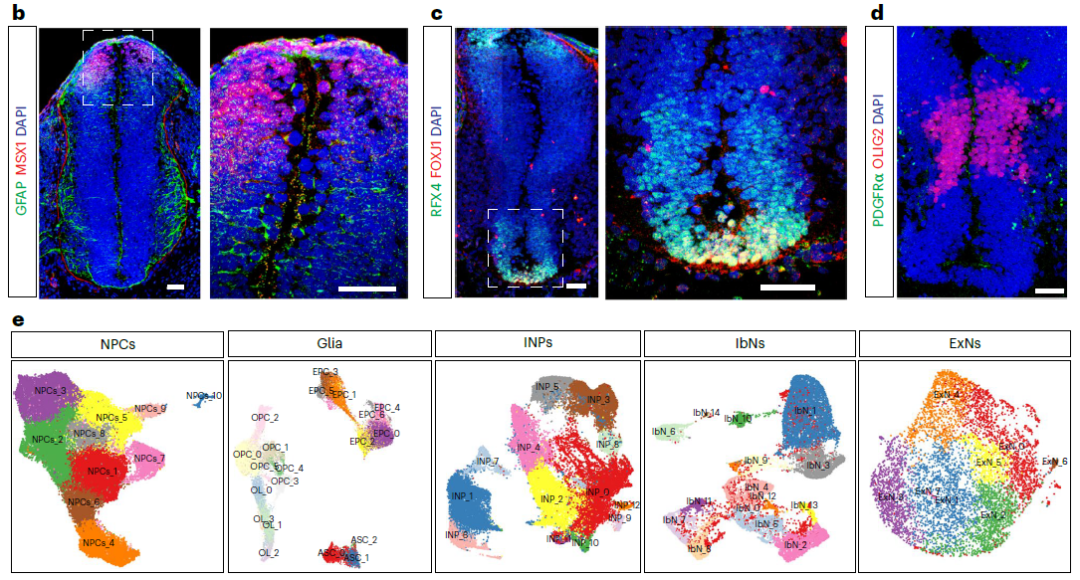
图2 脊髓神经细胞的异质性
3 hNPCs 分化受特定基因的调控
为了描述 NPC的 分化特征,从 scRNA-seq中选择了NPC 和神经元细胞群进行拟时序分析。Slingshot 揭示了NPC分化为多个神经元细胞,每个分支都有特定的基因表达(图 3a,b)。通过NPC(DCC 和 GADD45G)、神经元谱系相关基因(ExNs 中的 CACNA2D1、IbNs 中的 NRXN3 和 ChNs 中的 NEFL)和神经元基因(ExNs 中的 KCNIP4、IbNs 中的 ROBO3 和 ChNs 中的 SLC5A7)的表达,HybISS进一步验证了轨迹结果(图 3b)。整合了 scRNA-seq 轨迹和 ST 数据,结果显示 hNPCs 首先分化为 INPs,然后分化为不同的功能神经元(图 3c)。其中EBF1(ExNs)、PAX2(IbNs)和 SLC5A7(ChNs),在 ST中表现出偏向 DV 的表达,这与分化神经元类型的定位相关(图 3d)。PBX3 与所有三个神经元系都有关联,因此没有表现出特定 DV 模式(图 3d)。
对胶质细胞进行了类似的分析,结果表明所有三个胶质细胞系都起源于一个共同的 NPC 亚型,并具有特定的分支相关基因(例如 EPC 的 CNTNAP5、ASC 的 MSX1 和 OPC 的 HES6)(图 3e)。在空间上,这些基因与新生神经胶质细胞在同一区域表达(图 3f)。综合轨迹和 ST 数据显示,hNPCs 以特定的空间模式分化为神经胶质细胞--脊髓背侧为 ASCs,脊髓中央为 EPCs,脊髓腹侧为 OPCs 和 OLs(图 3g)。
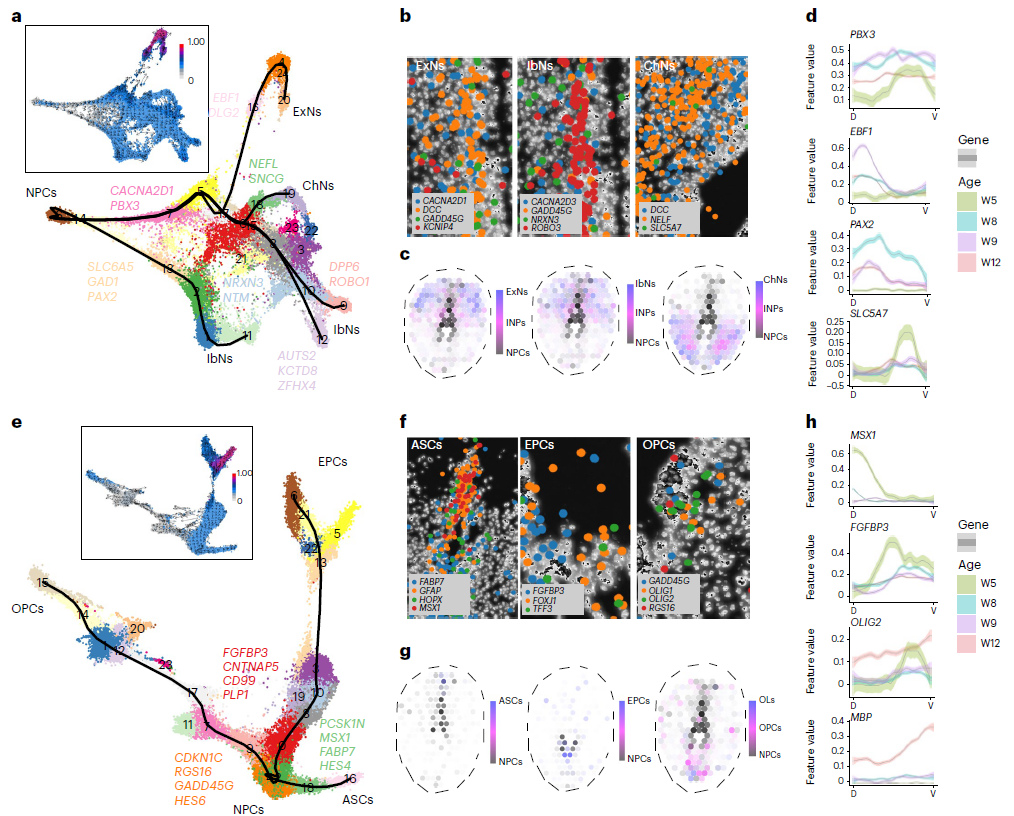
图3神经细胞和胶质细胞分化发育的时空调控
4 人类脊髓发育的调控网络
为了更好地理解沿 DV 轴的调控(如 TFs、信号通路和细胞-细胞相互作用),首先分析了神经相关的信号通路,发现大多数细胞类型都表达WNT、NOTCH 和 SHH的相关基因,但随着时间的推移而减少(图 4b)。IHC 证实,在W5时active-β-catenin (ABC)和 SHH 通路分子(SHH、GLI1 和 GLI3)显著表达,但 W8 后表达明显减少(图 4c)。
Progenitors相关基因在 W5 阶段表现出 DV 偏向表达,而Neurons相关基因在 W5-8 阶段表现出 DV 偏向表达(图 4e)。细胞共定位结果表明,NPC 的比例明显下降;在W5时,NPC分化为神经元和前神经胶质细胞;而在W8时,neurogenesis和gliogenesis细胞开始发生迁移(图4f)。
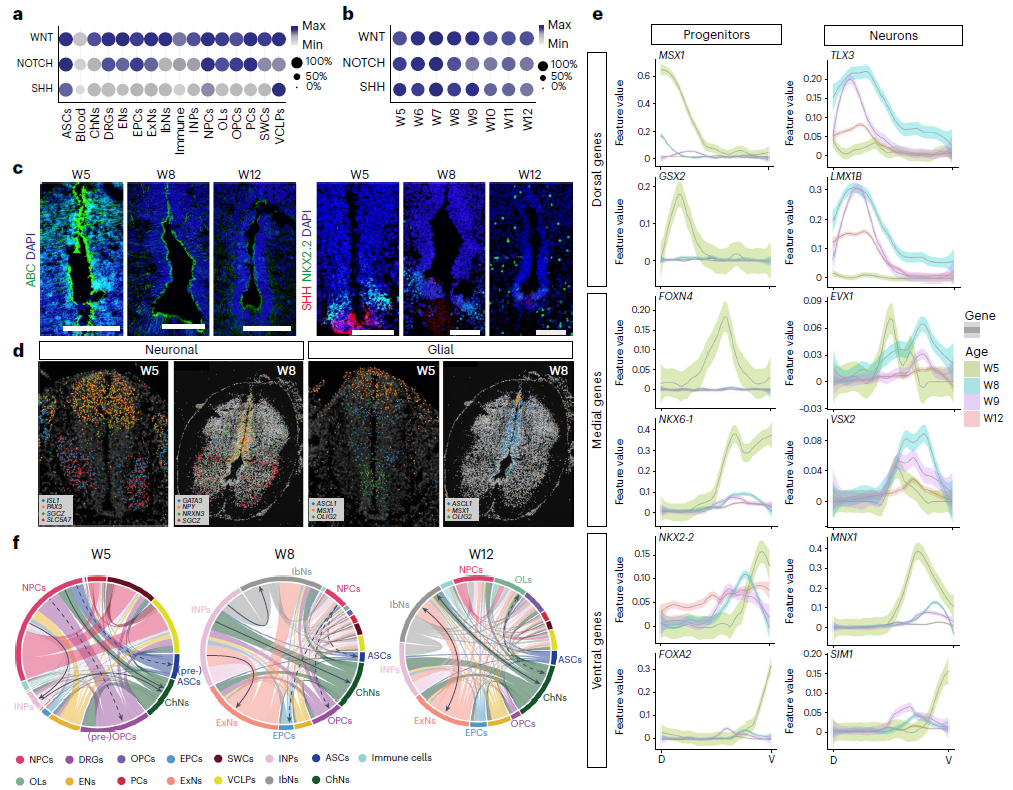
图4 人类脊髓发育的调控网络
5 小鼠和人类脊髓发育的异同
为了探讨低增殖的人NPC是否是一种特殊表型,将 scRNA-seq与两个小鼠脊髓发育数据集进行了整合分析(图 5a)。从 W5 到 W7,大多数 hNPCs 的增殖标记物 MKI67 和 TOP2A 表达量较低,与此形成鲜明对比的是,小鼠 NPCs(mNPCs)至少在胚胎 13.5 天(相当于人类的 W7 天)前增殖能力很强(图 5b)。IHC 显示,在 W5 人类脊髓中,许多 SOX9+ hNPCs 不表达 Ki-67,这与小鼠 E10.5 脊髓中大部分 Sox9+Ki-67+ 细胞不同。这证实,与 mNPCs 不同,大多数 hNPCs 在发育早期就进入了静止期(图 5c)。
在人鼠整合 scRNA-seq 数据集中,我们发现 MSX1、GFAP在人ASCs 中确实高表达,但在小鼠的 ASCs 中却低表达(图 5d)。相反,MSX1 和 FOXJ1 在小鼠和人类Ependymal 中均有表达,这表明 MSX1 在调节人类 ASC 和 EPC 的细胞命运过程中具有双重作用,但在小鼠中只调节 EPC。对人(W8)和小鼠(E16)脊髓切片在相似时间点的 ST 分析验证了 MSX1 在人中的表达主要位于背侧心室区,与 ASCs 中 GFAP 和 EPCs 中 FOXJ1 的标记基因表达相关(图 5e)。然而,在小鼠切片中,我们发现 Msx1 与 Foxj1+ 细胞在同一区域表达,但不在 Gfap+ 区域表达,这与之前的研究26 显示 Msx1 调控小鼠 EPC 发育的结果一致(图 5e)。总之,这些数据表明,小鼠和人类脊髓发育过程中的时空基因表达存在根本差异。
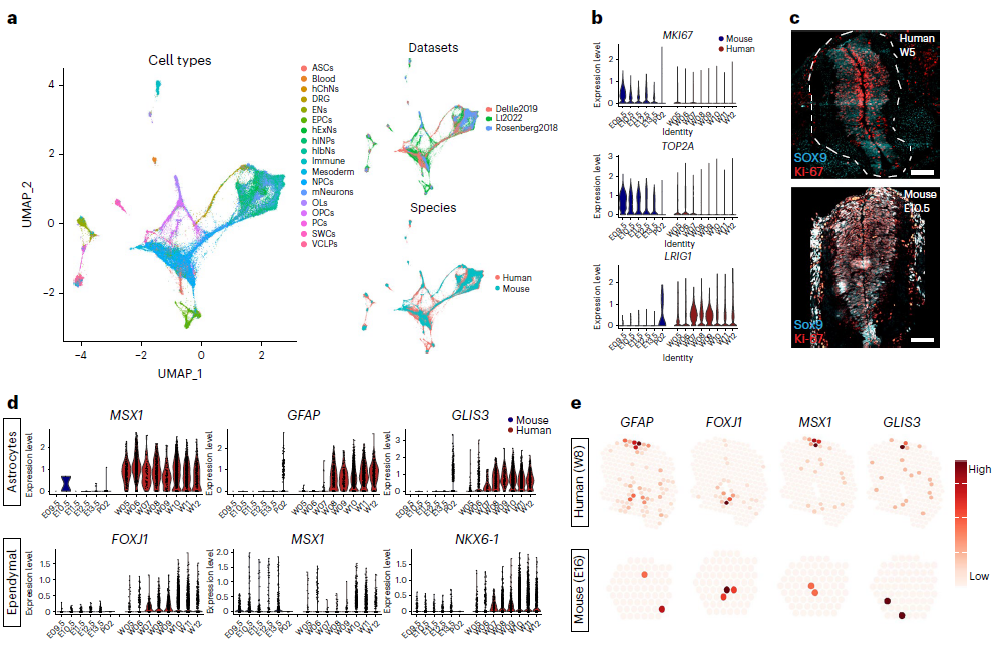
图5 神经发育过程中的物种特异性
6 揭示肿瘤特异性表达基因
将脊髓肿瘤单细胞数据映射到ST 数据上,发现脊髓肿瘤细胞广泛存在但无区域特异性基因,表明正常人发育中的脊髓中有许多细胞类型与肿瘤有相似之处(图 6a)。将 scRNA-seq与室管膜瘤单细胞转录组数据进行整合分析。尽管神经元和胶质细胞有不同程度的重叠(图 6c、f),但神经元标记基因主要在正常神经元中表达(图 6d),而胶质细胞的标志基因在正常细胞和肿瘤细胞中表达相似(图 6g)。
此外,重点比较了正常细胞和肿瘤细胞的重叠区域,发现了肿瘤特异性基因,如CASC15 和 microRNA MIR99AHG,RPS14 和 RPS8(图 6e,h)。许多 CSC 与正常 NPC 重叠(图 6i),并共同表达经典 NPC 标记 SOX2 和 VIM(图 6j)。发现了 CSC 特异性标记 FTX 和 MIR99AHG,它们在正常 hNPCs 中没有表达,因此可能成为室管膜瘤 CSC 的新治疗靶点(图 6i-k)。
为了进一步研究 hNPC 和 CSC 分化的分子差异进行拟时序轨迹分析,结果表明TF RFX2 和 RFX4与 EPC 分化高度相关(图 6l,m)。NLRP1 和 VWA3B 分别与正常 EPC 和 EPC 样 CSC 的分化特别相关(图 6n)。同样,WLS 和 APOD 分别与 ASC 和 OPC的分化相关(图 6o,p)。
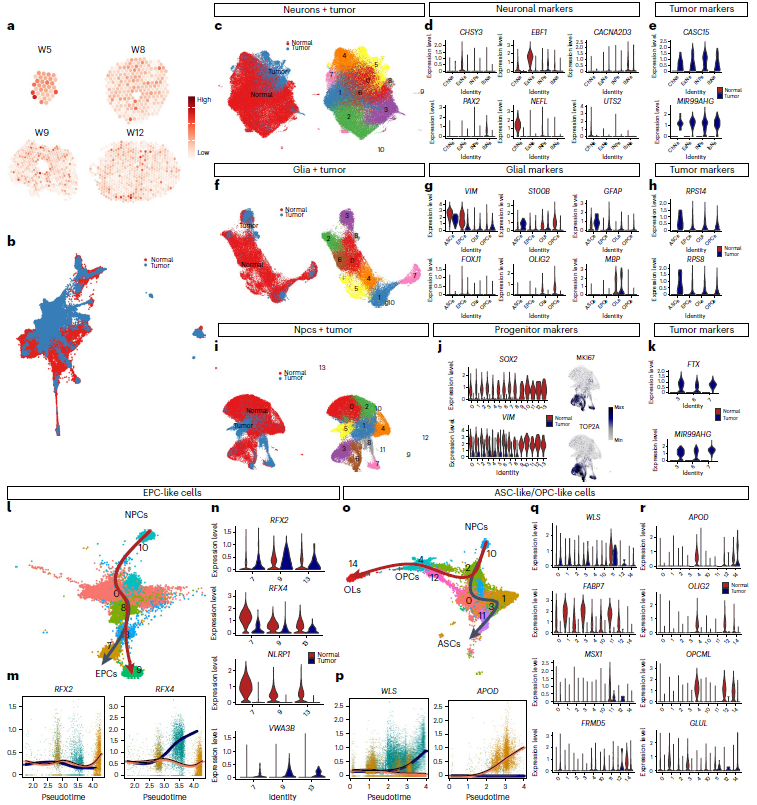
图6 胎儿脊髓与室管膜瘤的关系
总 结
该研究除了经典的细胞图谱分析,还从生物学方面进行了着重研究,包括:1)与小鼠经典发育模型(神经干细胞先是生成神经细胞,后再生成胶质细胞)不同,本研究发现人类神经干细胞几乎在同一时间段同时生成神经元与胶质细胞;2)使用三种方法进行单细胞测序发育轨迹分析且整合到空间转录组数据后,获得了神经干细胞分化成人类脊髓各类神经元与胶质细胞的调控基因以及分化过程中的细胞迁移路径;3)把人类脊髓发育的数据与儿童室管膜肿瘤的单细胞测序数据进行整合分析,发现了室管膜肿瘤干细胞发生发展与神经干细胞分化过程中的基因表达异同。最后,文章还提出一些基因在肿瘤干细胞中有特定表达,因此可以作为进一步肿瘤诊断与基因靶点的研究对象。
参考文献
Li X, Andrusivova Z, Czarnewski P, et al. Profiling spatiotemporal gene expression of the developing human spinal cord and implications for ependymoma origin. Nat Neurosci. 2023 May;26(5):891-901. doi: 10.1038/s41593-023-01312-9. PMID: 37095395; PMCID: PMC10166856.

业务咨询