上海和元生物技术(集团)股份有限公司品牌商
14 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
推荐产品
公司新闻/正文
Eur Heart J 葛均波院士/孙爱军教授团队与杨靖教授团队合作揭示HNMT介导的代谢-表观重塑调控病理性肥厚/心衰进展新机制
55 人阅读发布时间:2026-04-27 10:24
心力衰竭(HF)是多种心血管疾病的终末阶段,患者生存质量严重受损,病死率高居不下1。近年来,心衰药物治疗方案持续演进:从传统的抑制神经内分泌的“金三角”,到纳入钠-葡萄糖共转运蛋白2抑制剂的“新四联”,再到加入可溶性鸟苷酸环化酶激动剂的“五朵金花方案”,治疗策略不断丰富2。然而,即便在这些规范治疗之下,患者仍面临心衰进展与死亡风险的残余威胁。面对如此严峻的形式,亟需针对心衰的病理生理机制进行深入探索,挖掘心衰治疗的新靶点。
在心衰进展过程中,心肌细胞为适应能量需求,会发生复杂的代谢重塑。然而,当这种重塑走向失代偿,便成为推动心衰进展的核心动力。传统观点集中于脂肪酸氧化向葡萄糖利用的转化,但近年来,一系列更基础的“代谢中间产物”被发现能直接改变细胞表观遗传修饰,从而深度调控基因表达3。这提出了一个关键科学问题:在衰竭的心脏中,是否存在某种关键代谢物的变化,通过“重写”表观遗传密码,最终锁定了心肌细胞的病理性命运?
组胺,一种经典的炎症介质,在心脏中同样扮演着复杂的信号角色,其稳态依赖于合成与清除的平衡4。组胺N-甲基转移酶(HNMT)是心脏中清除组胺的关键代谢酶,它以一种独特的“消耗型”方式工作:每代谢一份子组胺,就必须消耗一份子S-腺苷甲硫氨酸(SAM)。SAM是细胞内最重要的通用甲基供体,是维持DNA和组蛋白甲基化修饰的基石5。本研究发现HNMT在心衰时表达上调,这引出了一个极具吸引力的科学假设:在心力衰竭中,HNMT的上调是否会像“黑洞”一样消耗SAM,导致细胞陷入“甲基耗竭”,进而引发广泛的表观遗传失调,最终驱动心衰进展?
近期,复旦大学附属中山医院葛均波院士、孙爱军教授团队联合徐汇区中心医院杨靖教授团队在European Heart Journal杂志(IF=35.6)上在线发表题为“Histamine N-methyltransferase upregulation, cardiac hypertrophy, and heart failure”的研究论文,揭示了HNMT在HF中的核心作用及调控机制,为疾病治疗提供了新的干预靶点。

研究团队首先通过蛋白质谱技术、临床样本分析与动物模型验证发现,无论是心衰患者的心脏组织,还是经主动脉弓缩窄术(TAC)诱导的小鼠心衰模型心脏组织中,HNMT的表达水平均显著上调。公共单细胞数据分析表明,HNMT主要在心肌细胞表达。在细胞层面,phenylephrine(PE)刺激可显著诱导原代心肌细胞中HNMT的表达升高。此外,研究团队还发现心衰患者尿液中的N-甲基组胺(HNMT的下游代谢物)显著升高,且其浓度与心功能指标呈负相关,这提示尿液中的N-甲基组胺具有作为心衰无创生物标志物的潜力。
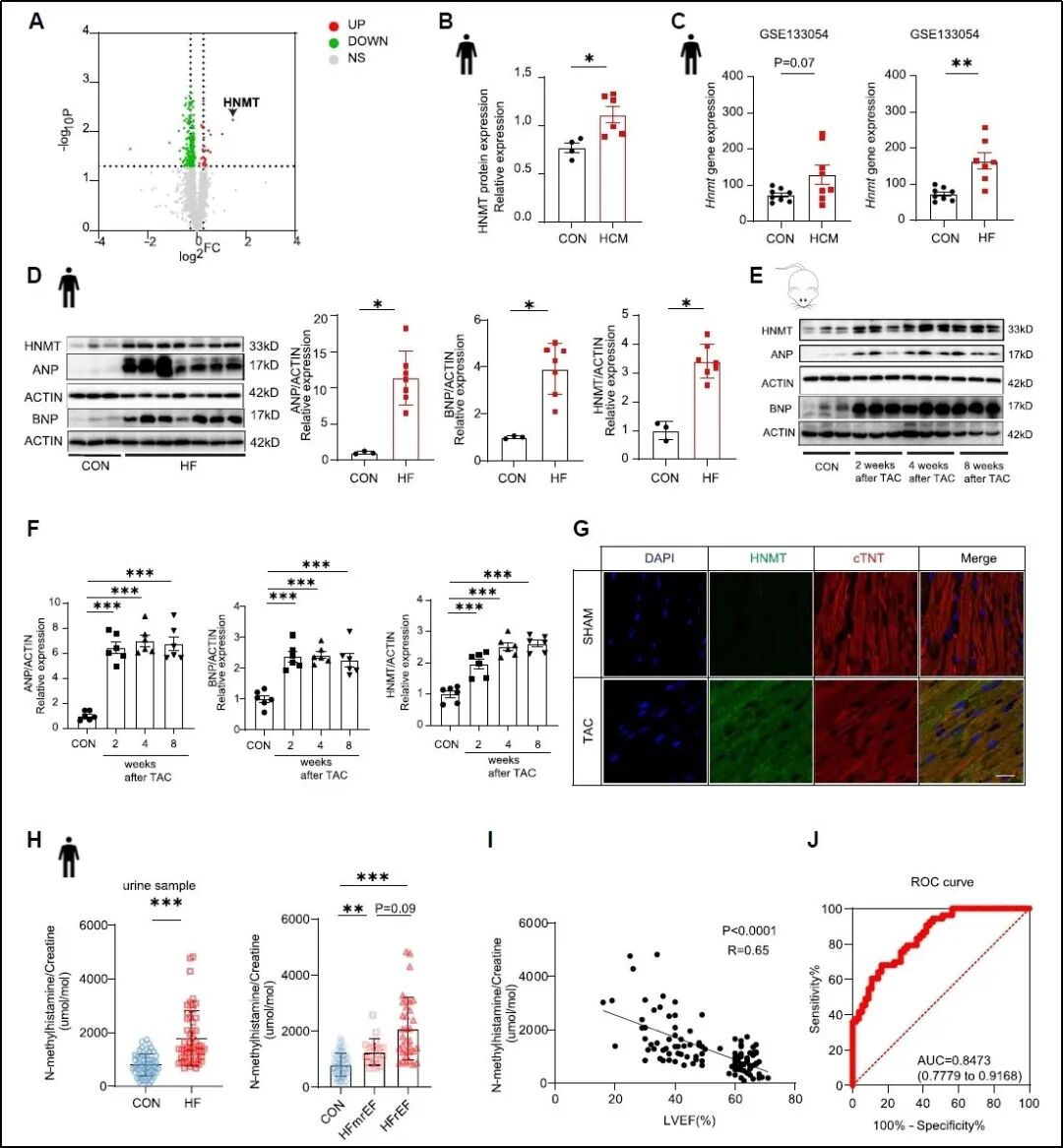
图1. 心肌细胞HNMT在心衰时显著上调
为了探究HNMT在心力衰竭中的作用,研究团队构建了心肌细胞特异性HNMT敲除小鼠,采用TAC术诱导心衰。术后心超及组织染色分析显示,HNMT敲除显著减轻了TAC引起的心肌病理性肥厚,并改善了心脏收缩功能。进一步地,团队利用携带心肌细胞特异性启动子的AAV9载体在心肌细胞中特异性过表达HNMT,发现即使在不施加额外压力负荷的情况下,单纯过表达HNMT即足以引发心功能损害。 此外,研究人员对原代心肌细胞进行了腺病毒介导的HNMT过表达(Adv-Hnmt)和敲低(Adv-shHnmt)处理。结果显示HNMT的过表达足以在无外部刺激的情况下诱导细胞肥大;相反,在PE诱导的压力条件下,HNMT敲低显著减弱了细胞肥大的反应。这表明HNMT在体外也能够调节心肌细胞肥大。
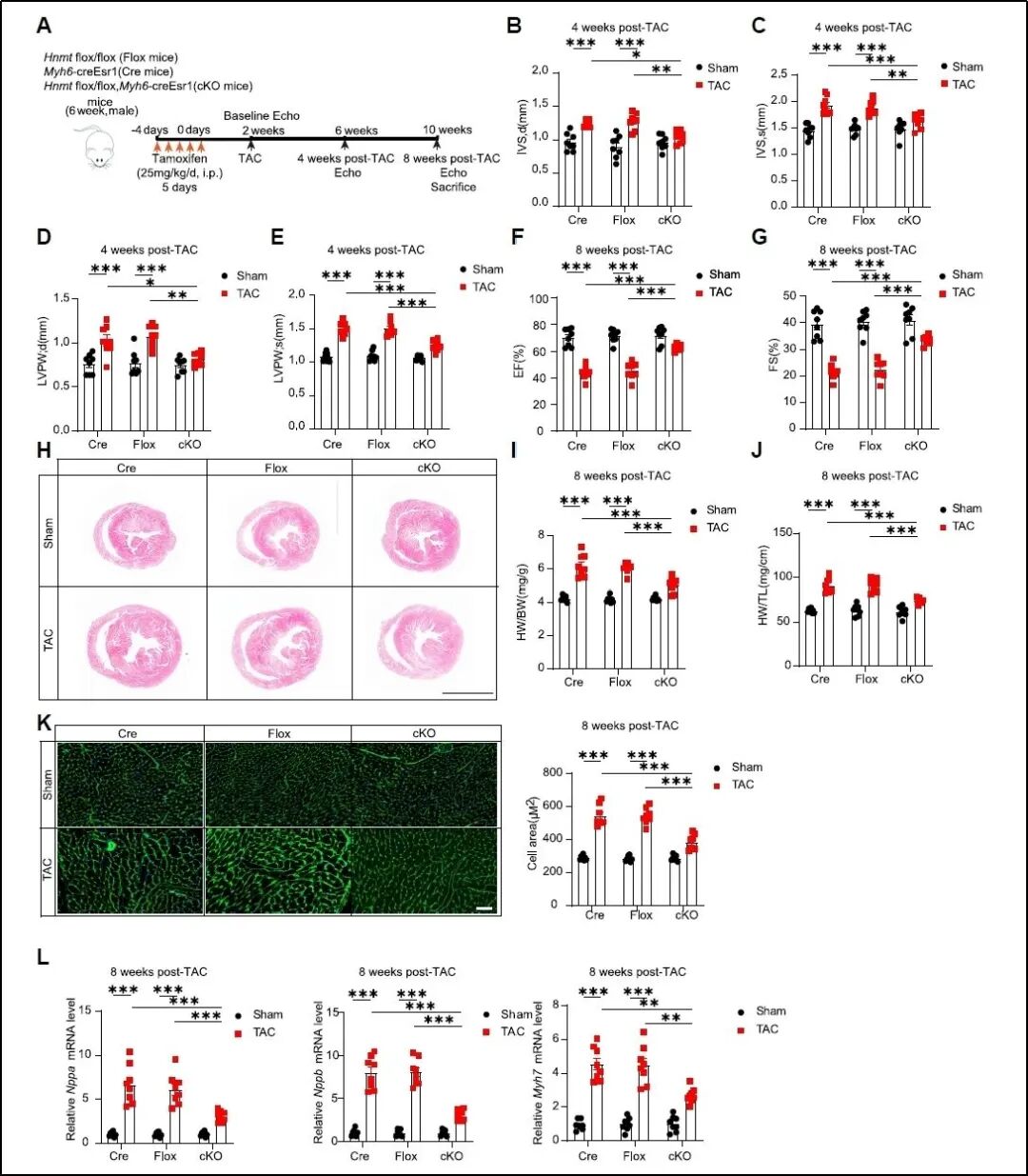
图2. 心肌特异性HNMT敲除可以缓解TAC导致的心功能障碍
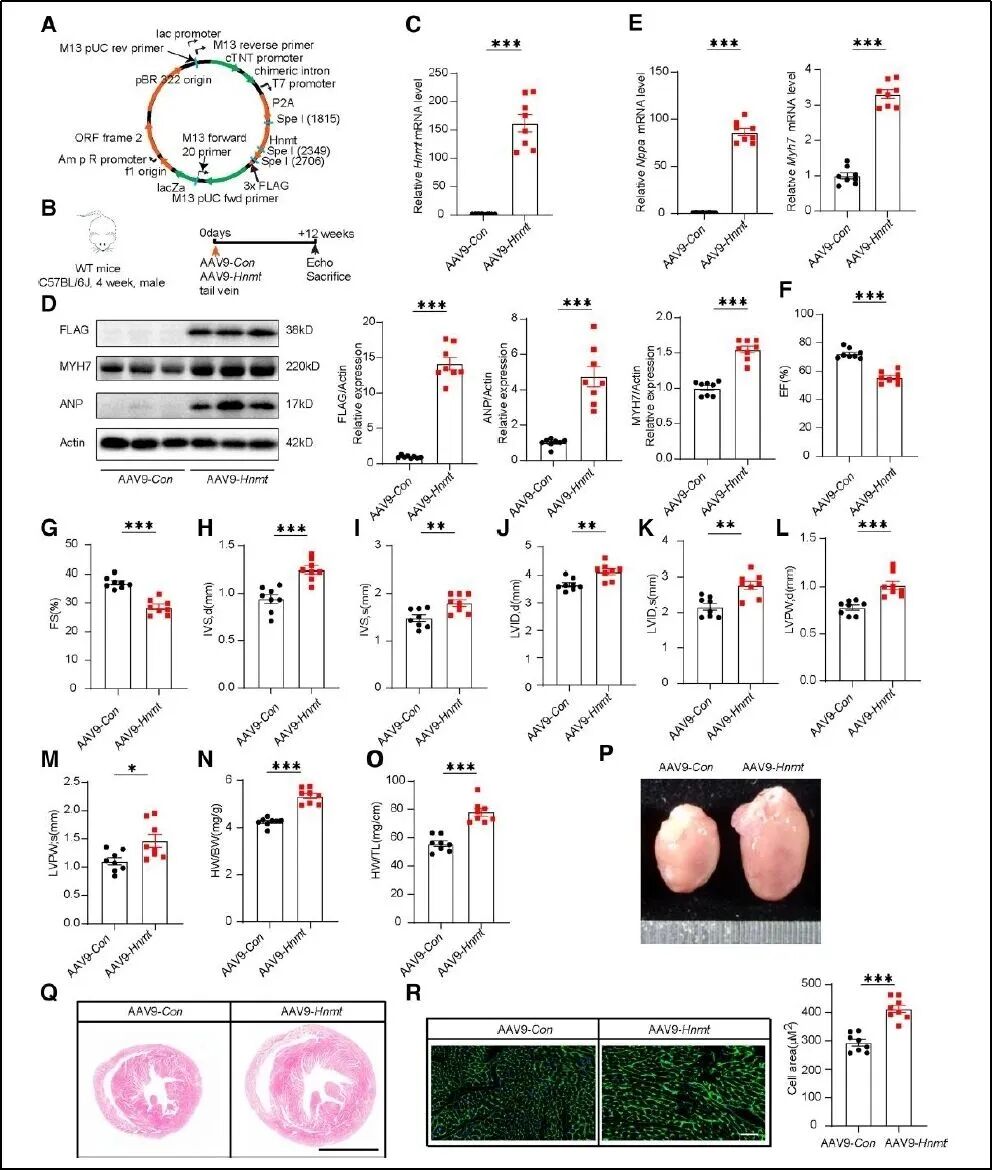
图3. 心肌特异性HNMT过表达可以导致心功能障碍
为阐明HNMT导致心功能损害的具体分子机制,研究团队对经HNMT敲低或过表达处理的原代心肌细胞进行了转录组测序分析。RNA-seq结果提示,WNT/钙离子信号通路很可能是HNMT调控的关键下游。后续功能实验进一步明确,HNMT主要激活了非经典WNT信号中的WNT/CaMKII分支,而对经典WNT/β-catenin通路及平面细胞极性(WNT/PCP)通路则无明显影响。
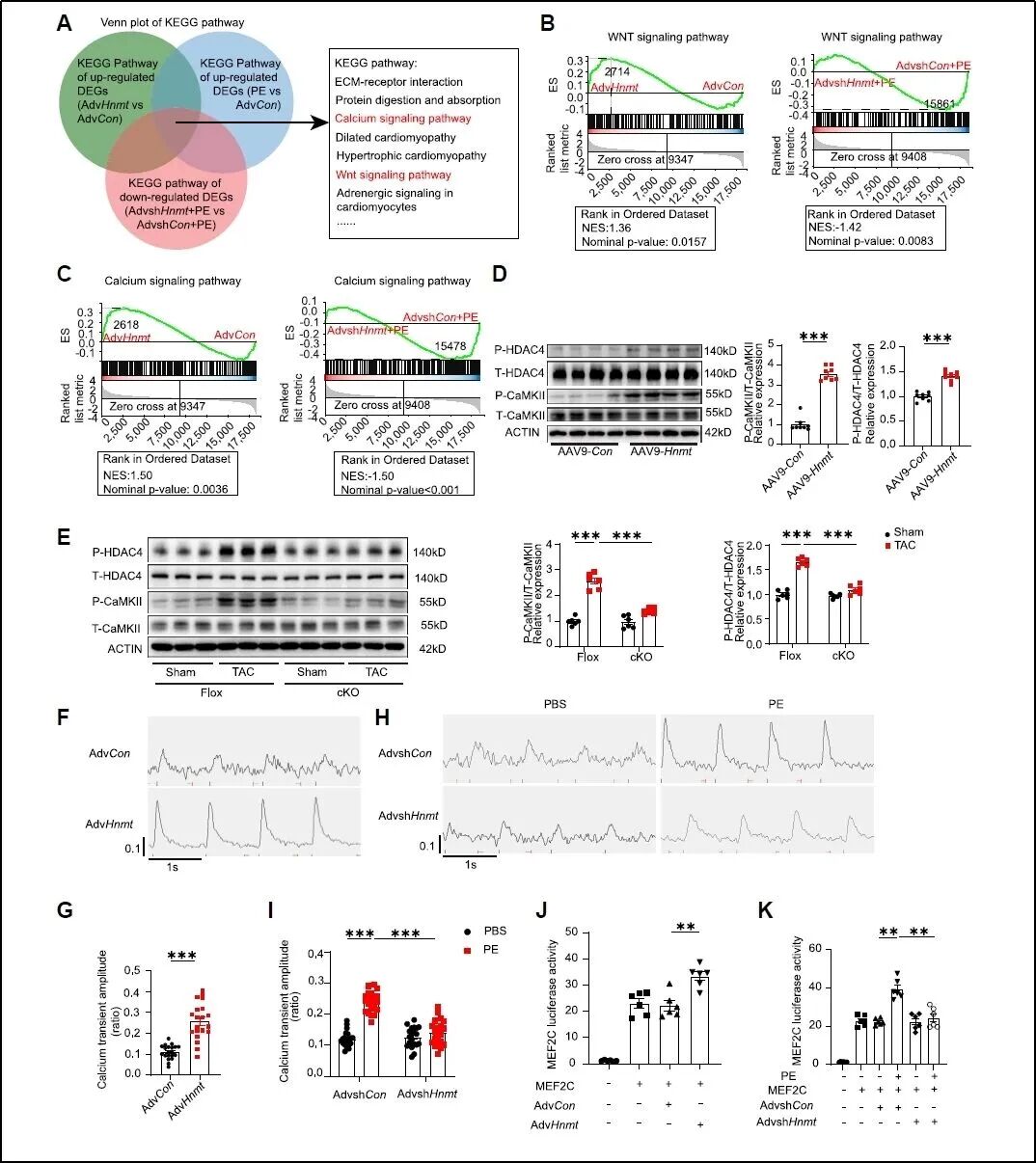
图4. HNMT调控WNT/CaMKII通路
鉴于HNMT作为一种代谢酶的功能特性,研究团队推测其可能通过改变细胞内特定代谢物的水平来调控WNT/CaMKII通路。基于靶向代谢组学分析,发现过表达HNMT可导致心肌细胞中其下游代谢物SAM (S-adenosylmethionine)含量显著降低,而敲低HNMT则能逆转PE诱导的SAM水平下降。进一步的实验证实,外源性补充SAM可有效逆转HNMT过表达所导致的WNT/CaMKII通路激活,并改善由此引发的心功能损害。
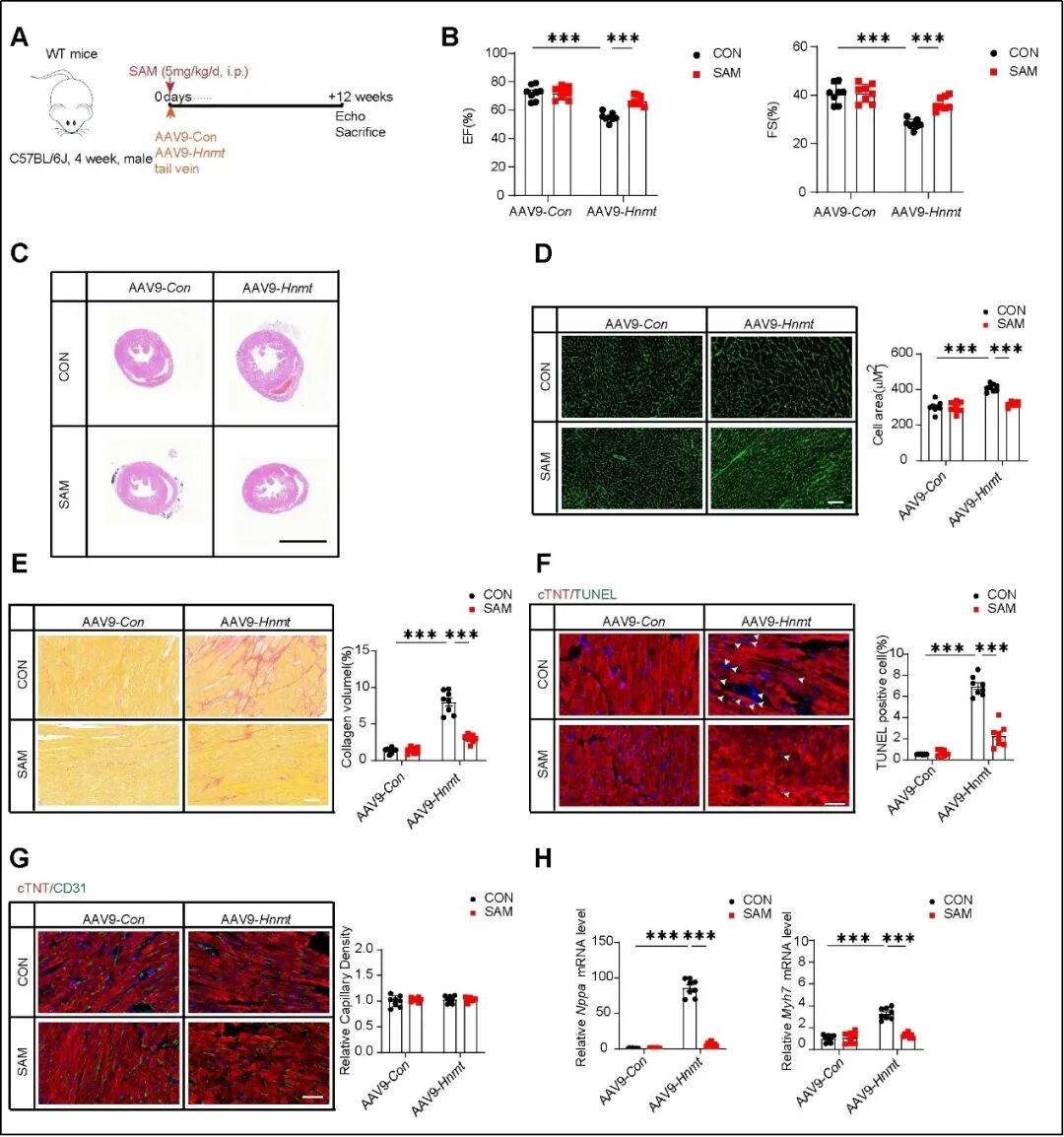
图5. SAM回补可以逆转HNMT过表达导致的心功能障碍
由于SAM是细胞内关键的甲基化修饰底物,研究团队进一步探究了HNMT是否通过影响蛋白甲基化状态来发挥作用。通过泛甲基化抗体检测结合核质分离技术,发现过表达HNMT后,位于组蛋白分子量对应区域的甲基化信号显著减弱(详见补充材料)。基于组蛋白甲基化修饰组学分析与后续实验验证,团队锁定H3K27三甲基化(H3K27me3)是受HNMT调控的核心组蛋白修饰。进一步的机制研究表明,HNMT能够直接与EZH2 (多梳抑制复合体PRC2的核心催化亚基,负责催化H3K27me3修饰并介导基因沉默)结合。该相互作用的证实,从分子层面解释了HNMT为何能够特异性扰动H3K27me3修饰水平。
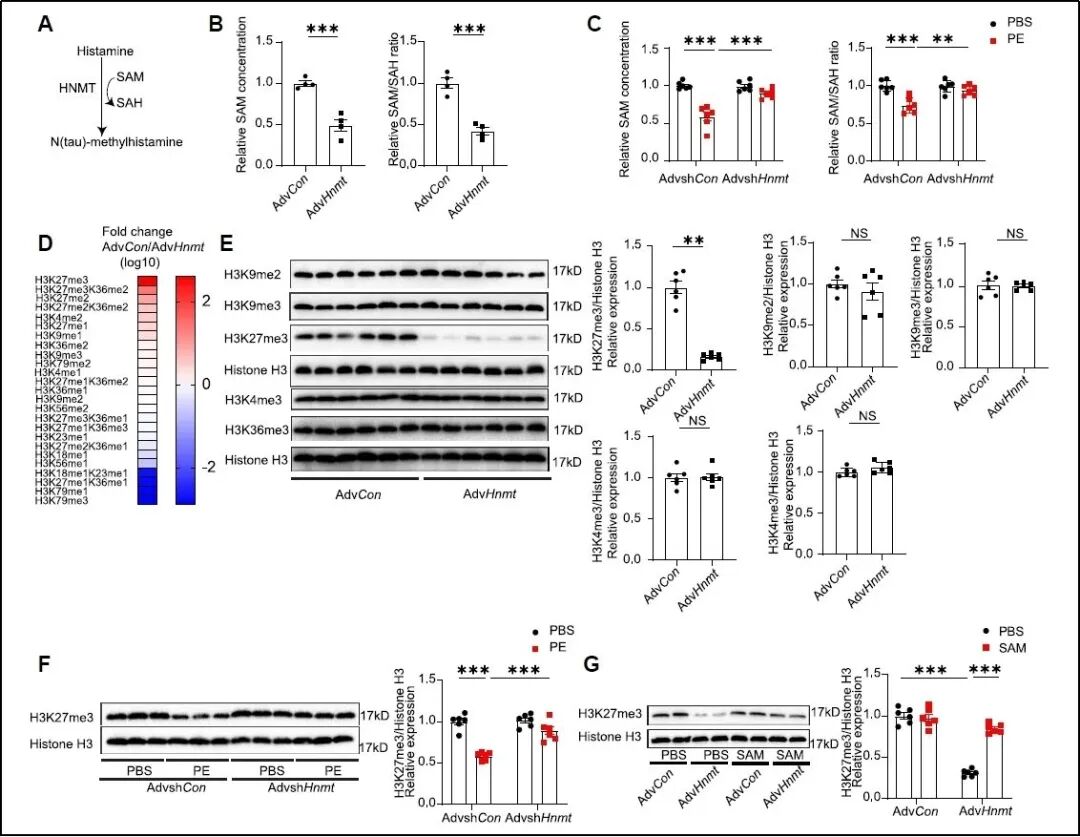
图6. HNMT调控H3K27me3修饰
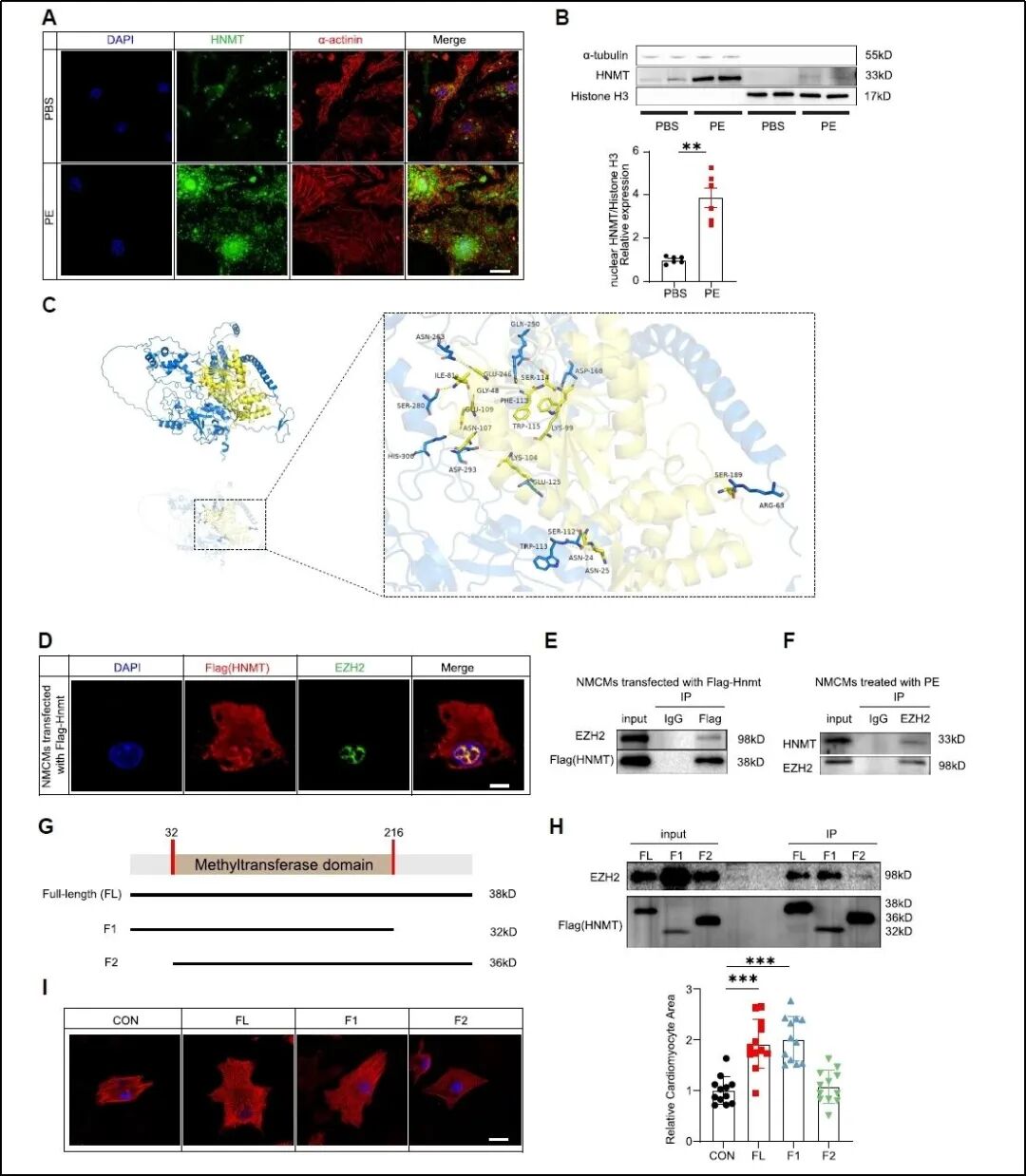
图7. HNMT可以结合EZH2
为了探究HNMT如何通过影响H3K27me3修饰调控WNT/CaMKII通路,研究团队运用CUT&Tag测序技术在全基因组范围内检测了H3K27me3的富集情况。通过整合CUT&Tag与RNA-seq数据,团队发现FZD2—WNT/CaMKII通路的一个关键基因—其启动子区域的H3K27me3修饰水平受HNMT特异性调控。进一步实验证实,过表达HNMT可显著降低FZD2启动子区的H3K27me3占据,从而解除对该基因的转录抑制,促使FZD2表达上调,进而激活WNT/CaMKII信号轴,最终导致心脏功能恶化。 研究人员在体外使用腺病毒(Adv-shFzd2)以及在体内使用AAV9(AAV9-shFzd2)来敲低Fzd2基因,体内外实验均证明FZD2敲低可以缓解HNMT过表达所引起的心功能障碍。
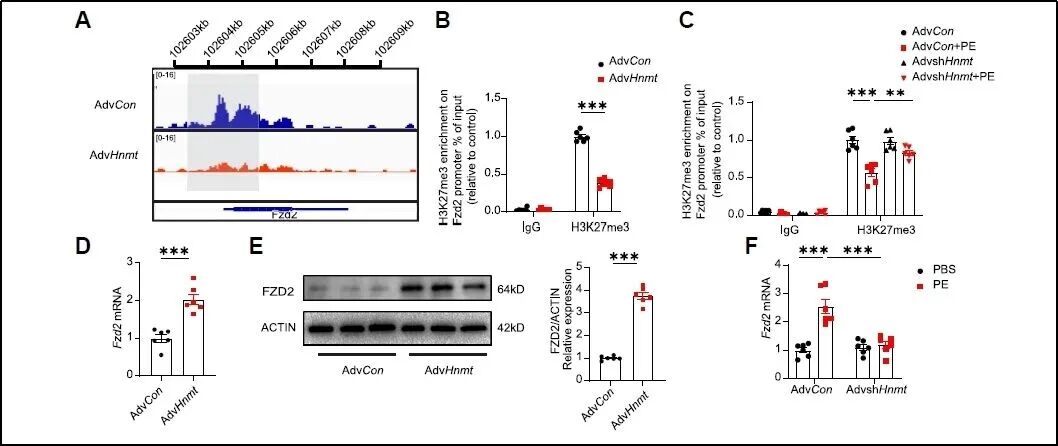
图8. HNMT调控FZD2启动子区域的H3K27me3修饰,从而促进FZD2转录
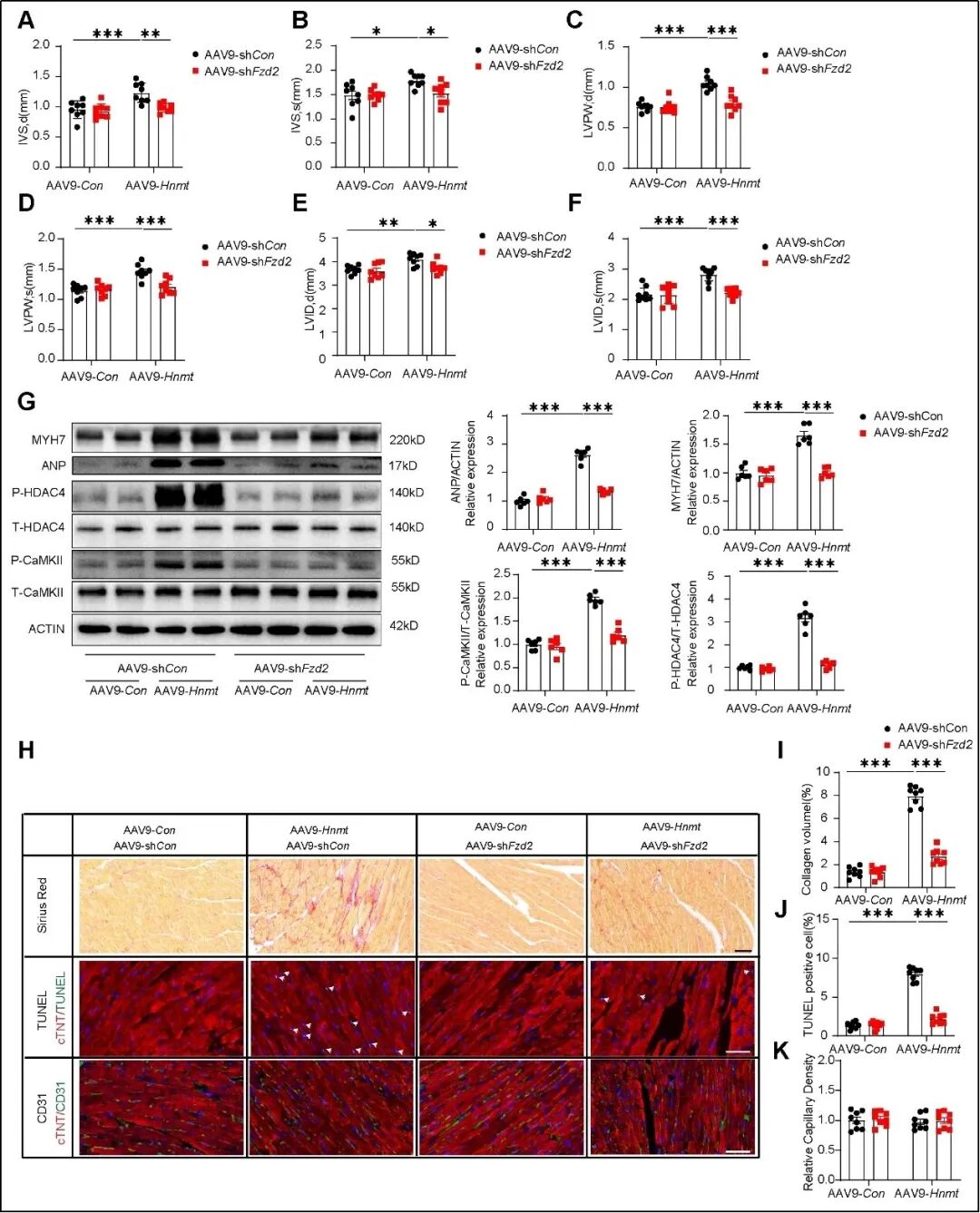
图9. FZD2敲低可以缓解HNMT过表达导致的WNT/CaMKII通路激活以及心功能障碍
最后,研究团队利用阿莫地喹(HNMT抑制剂)干预TAC小鼠,发现阿莫地喹能够有效改善小鼠心功能。
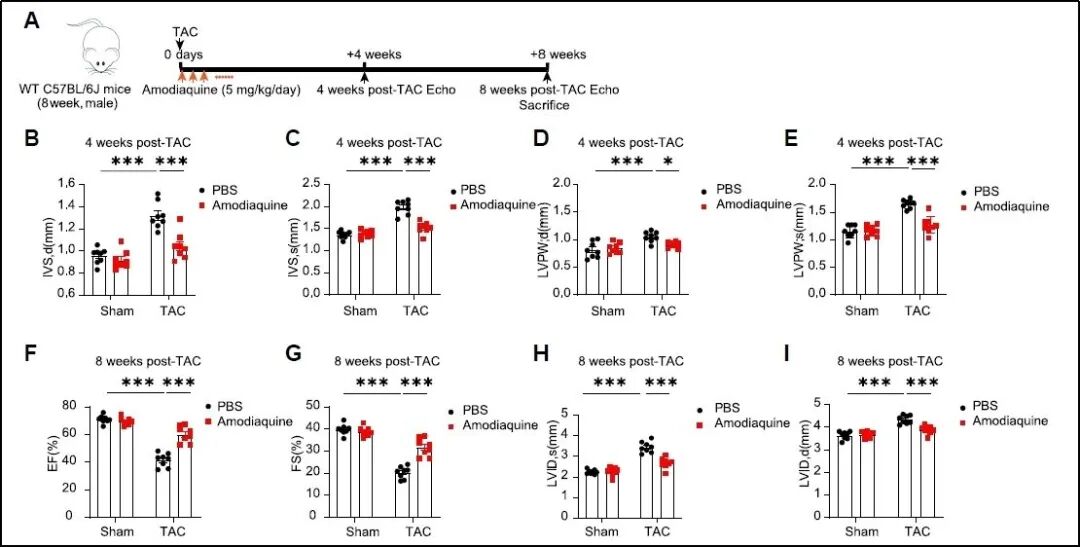
图10. 阿莫地喹可以缓解TAC导致的心功能障碍
综上所述,本研究系统揭示了HNMT是驱动心力衰竭进展的关键分子,其机制可概括为:HNMT通过消耗细胞内SAM,并与EZH2结合干扰其功能,特异性降低FZD2启动子区域的H3K27me3修饰水平,从而解除对FZD2的转录抑制,激活下游WNT/CaMKII信号通路,最终导致心功能进行性恶化。在临床转化方面,研究团队发现:1. 尿液中的N-甲基组胺(HNMT的下游代谢产物)具有作为心衰无创诊断新标志物的潜力;2. 传统的抗疟疾药物—阿莫地喹(HNMT抑制剂)可以改善心衰小鼠心功能。阿莫地喹作为一种已广泛应用于临床的抗疟药物,其长期用药安全性已得到验证,迄今未见与严重心血管不良事件相关的明确报道6,这为其“老药新用”提供了可靠的安全性基础与转化优势,相关临床验证计划正在积极筹划中。
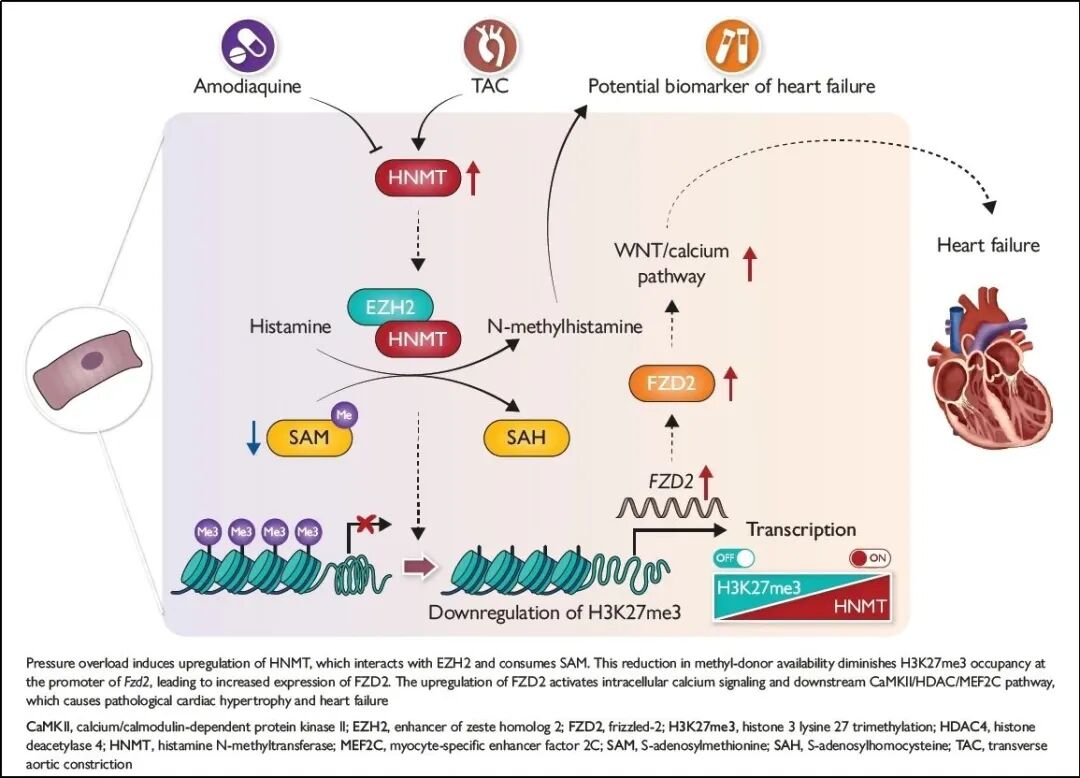
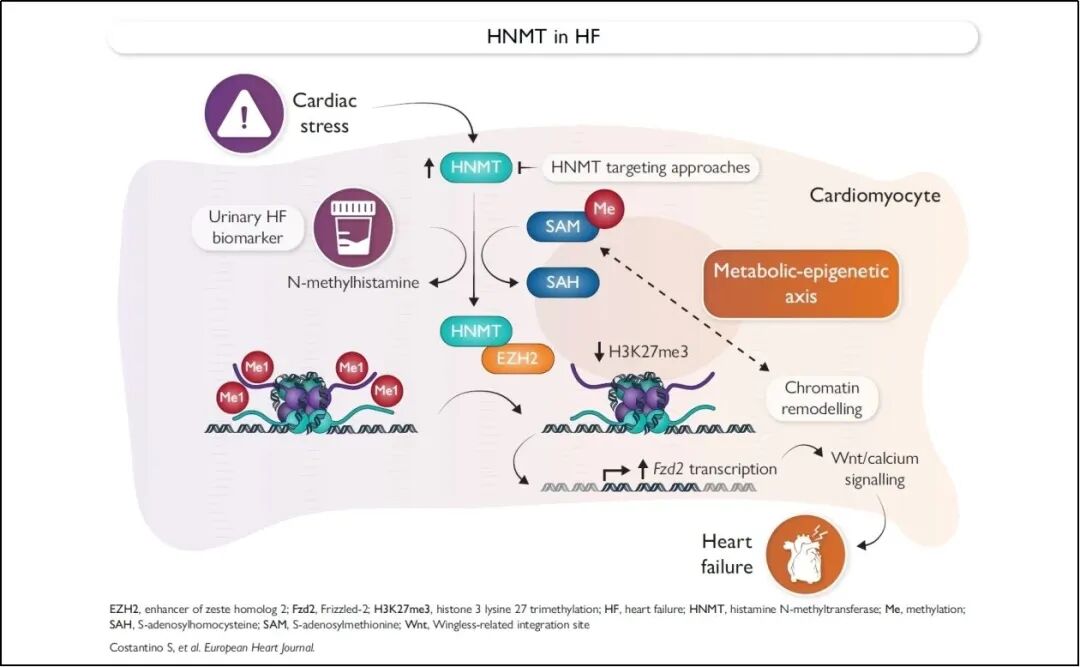
同期,苏黎世大学心脏病学教授、心脏病学系转化与实验心脏病中心(CTEC)主任Francesco Paneni教授撰写发表了题为“Histamine N-methyltransferase in heart failure: from metabolic signalling to chromatin remodelling”的编者按评价,对该研究进行了充分肯定:“这是一项重要的研究,揭示了一种新的信号机制以及一个潜在的可药物靶点,用于调节衰竭心脏中的SAM水平和表观遗传重塑。”
该研究由复旦大学附属中山医院葛均波院士、孙爱军教授和上海市徐汇区中心医院杨靖教授共同指导完成,中山医院章金延博士后、蒋昊主治医师、刘历威博士后,徐汇区中心医院李昕硕士为论文共同第一作者。该工作得到国自然基础科学中心(T2288101)、国自然重点项目(82130010)等项目资助。该工作特别感谢复旦大学特聘教授胡凯教授在项目设计及论文返修期间的精心指导。同时,衷心感谢复旦大学李立亮教授、复旦大学附属中山医院徐磊副主任医师、徐亚妹副主任医师、金雪娟教授的大力支持。
和元助力
和元生物有幸为研究者提供用于小鼠体内实验的AAV,以及体外细胞实验的腺病毒载体。和元生物以实际行动助力心血管研究!



更多活动详情可长按或扫描上方二维码,填写表单,我们将尽快安排专人与您联系!
和元生物
和元生物成立于2013年,作为深耕细胞和基因治疗核心领域的高新技术企业,专注于为细胞和基因治疗的基础研究提供基因治疗载体研制、基因功能研究、药物靶点及药效研究等CRO服务,可提供①组学服务:常规转录组、单细胞转录组、基因组、代谢组及蛋白组等。②载体构建和病毒包装:质粒、siRNA、腺相关病毒(AAV)、腺病毒(ADV)、慢病毒(LVV)、逆转录病毒(RV)、单纯疱疹病毒(HSV)等病毒载体生产服务,提供R&D、实验室级别、GMP级别满足研发、小动物、大动物NHP到临床的不同研究阶段的使用需求。③细胞实验服务:过表达、干扰稳定株构建,单克隆细胞株构建服务及细胞功能学、药效学实验服务。④动物实验及机制研究:神经、代谢、肿瘤动物模型、药效药代、病理切片及蛋白、核酸检测服务。⑤特色项目服务:CRISPR文库筛选服务,外泌体整体研究服务,AAV衣壳筛选服务、听力研究整体项目服务,满足客户定制化或一站式项目服务,助力基础科学研究,促进基础研究到临床转化应用,推动细胞和基因治疗行业发展。