和元生物技术(上海)股份有限公司品牌商
14 年
手机商铺
- NaN
- 0.5
- 0.5
- 1.5
- 0.5
推荐产品
公司新闻/正文
Adv Mater|单细胞RNA测序指导设计的多酶水凝胶可用于糖尿病下颌骨缺损的再生修复
316 人阅读发布时间:2025-06-20 10:19
传统的骨组织工程材料很难在糖尿病下恢复生理性骨重塑,主要是由于促炎巨噬细胞向抗炎巨噬细胞的极化受损。
2024年10月22日,上海交通大学李方园、凌代舜和浙江大学俞梦飞共同通讯在Advanced Materials发表了题为“A Single-Cell RNA Sequencing Guided Multienzymatic Hydrogel Design for Self-Regenerative Repair in Diabetic Mandibular Defects”的研究论文。利用单细胞RNA测序技术,揭示了糖尿病生理性骨重塑过程中,一氧化氮(NO)和活性氧(ROS)在阻碍巨噬细胞复极化过程中的关键作用。基于此,研究团队设计了一种多酶骨组织工程水凝胶支架(MEBTHS),该支架由甲基丙烯化明胶水凝胶与钌纳米酶整合而成,具有Ru0和Ru4+成分,有助于通过Ru0高效消除NO,同时Ru4+表现出ROS清除性能。因此,MEBTHS通过中和ROS、逆转NO介导的线粒体代谢来协调巨噬细胞重编程,从而使糖尿病下颌缺损内的骨髓间充质干细胞和内皮细胞恢复活力,产生质量与正常骨相当的新生骨。
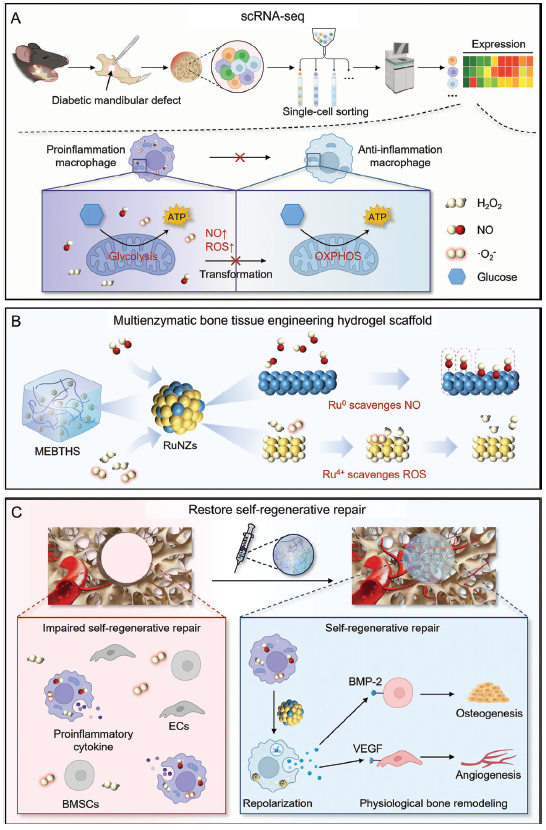
图1 MEBTHS协调巨噬细胞重编程以促进糖尿病下颌骨缺损的自我再生修复示意图
研究结果
1
巨噬细胞复极化在糖尿病下颌缺损中的作用机制
采用scRNA-seq技术来描绘正常小鼠和糖尿病小鼠下颌缺损愈合过程的差异。巨噬细胞可分为巨噬细胞1、巨噬细胞2和巨噬细胞3这3个细胞亚群。观察到巨噬细胞亚型比例发生了显著变化,强调了它们在愈合过程中的关键作用(图2A,B)。与正常小鼠相比,糖尿病小鼠下颌骨巨噬细胞1和巨噬细胞2(促炎特征)的细胞比例明显增加,巨噬细胞3(抗炎特征)明显下降。
糖尿病小鼠巨噬细胞的一个显著特征是诱导型一氧化氮合酶(iNOS)的高表达(图2C,D),导致大量NO的释放。值得注意的是,促炎巨噬细胞主要依靠糖酵解进行代谢,而抗炎巨噬细胞则倾向于OXPHOS,并伴有三羧酸循环中间体水平升高(图2E)。这些结果表明,在糖尿病下颌缺损中,NO通过抑制OXPHOS抑制促炎巨噬细胞向抗炎巨噬细胞的再极化。GO富集分析进一步强调了促炎巨噬细胞与炎症、ROS和NO生成的关联(图2F)。因此,NO和ROS在抑制糖尿病患者生理性骨重塑过程中的巨噬细胞复极化中起着至关重要的作用。
细胞间通讯分析显示,糖尿病小鼠的促炎巨噬细胞通过炎症信号通路抑制成骨细胞功能,包括Tnf、Sema4d和Il1b(图2G,H)。此外,在糖尿病小鼠中,由akr1c相关炎症信号通路介导的促炎巨噬细胞与内皮细胞之间的相互作用显著增强,表明促炎巨噬细胞通过趋化因子作用损害了糖尿病微环境中内皮细胞的血管生成能力。巨噬细胞、成骨细胞和内皮细胞之间的炎症串扰阻碍了成骨和血管生成,表明抑制巨噬细胞复极化损害了糖尿病微环境中的骨愈合。这些结果强调了清除NO和ROS对巨噬细胞重编程的必要性,以恢复糖尿病背景下的生理性骨重塑。
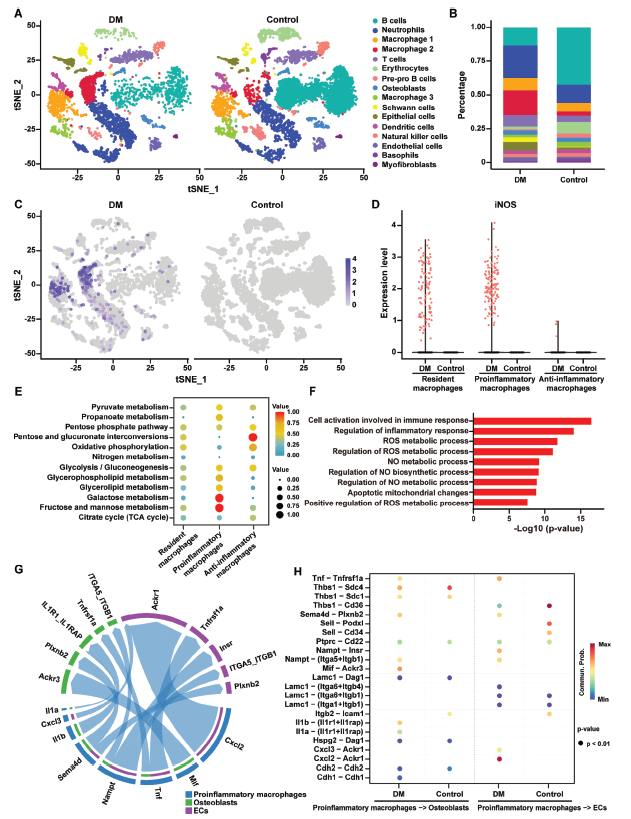
图2 应用scRNA-seq研究糖尿病生理性骨重塑过程中巨噬细胞复极化的机制
2
MEBTHS的设计与表征
Ru 纳米酶(RuNZs):RuNZs的设计主要基于其多酶活性,具备超氧化物歧化酶(SOD)和过氧化氢酶(CAT)的仿酶活性,可有效清除活性氧(ROS)和一氧化氮(NO)。特别是通过DFT计算发现,Ru0易与NO结合,通过形成稳定的Ru-N键来实现NO清除,主要用于降低糖尿病环境中的氧化应激。
GelMA 水凝胶:作为支架材料,GelMA在结构上与RuNZs结合形成多酶活性水凝胶MEBTHS。GelMA在骨缺损中可提供机械支撑,同时其良好的生物相容性使其适合用于组织修复 。
MEBTHS:通过结合RuNZs和GelMA,MEBTHS不仅具备高效的NO和ROS清除能力,还能在高氧化应激条件下稳定保持多酶活性。MEBTHS通过清除炎症环境中的ROS和NO,有效调节巨噬细胞极化,促进骨骼再生 。
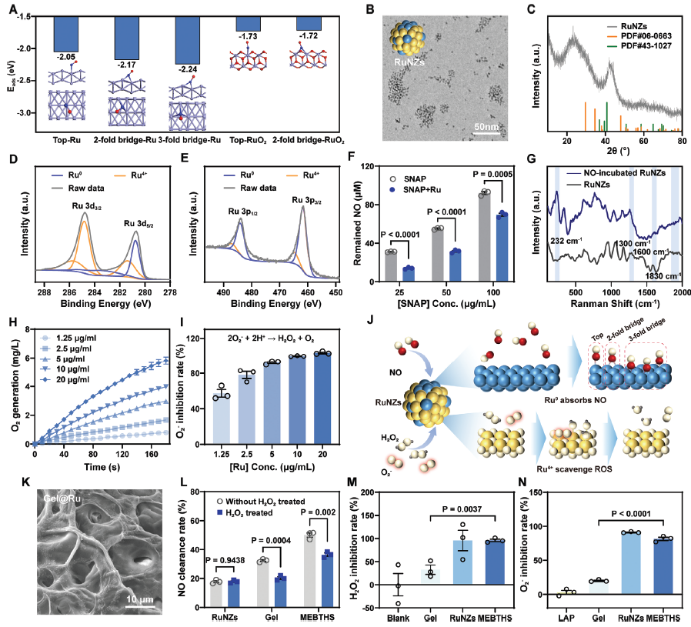
图3 设计了具有多酶活性的MEBTHS的合成及表征
3
MEBTHS通过同时清除NO和ROS促进巨噬细胞再极化
MEBTHS中的RuNZs可以很容易地内化到巨噬细胞中(图4A),并有效清除细胞内NO和ROS(图4B)。相比之下,凝胶仅能轻微降低细胞内NO和ROS水平,证实了MEBTHS具有出色的多酶活性。MEBTHS治疗后,促炎巨噬细胞(CD86)数量明显减少,而抗炎巨噬细胞(CD206)数量明显增加(图4C,D),表明MEBTHS具有将促炎巨噬细胞转化为抗炎巨噬细胞的能力。ELISA结果显示,MEBTHS显著降低了促炎细胞因子(IL-6和IL-1)的分泌,同时显著增加了抗炎细胞因子(IL-10和TGF-β)的分泌(图4E,F)。总的来说,MEBTHS通过多酶活性有效清除NO和ROS,促进巨噬细胞复极化,减轻炎症。
此外,还研究了MEBTHS通过清除NO和ROS重编程巨噬细胞的潜在机制。糖尿病微环境中一氧化氮水平升高通过抑制线粒体ACO2活性和增强SDH功能改变巨噬细胞线粒体电子传递链(图4G,H)。更糟糕的是,这种改变通过过量生产的fros,从而通过上调iNOS表达来放大NO的形成(图4I),从而阻碍巨噬细胞的再极化。给予MEBTHS治疗后,巨噬细胞中ACO2和SDH的活性恢复到正常水平。这种恢复以及iNOS表达的下调促进了线粒体功能的恢复(图4J)和巨噬细胞复极化。综上所述,这些发现表明MEBTHS能够同时清除NO和ROS,是一种有效的治疗糖尿病巨噬细胞复极化的药物(图4K)。
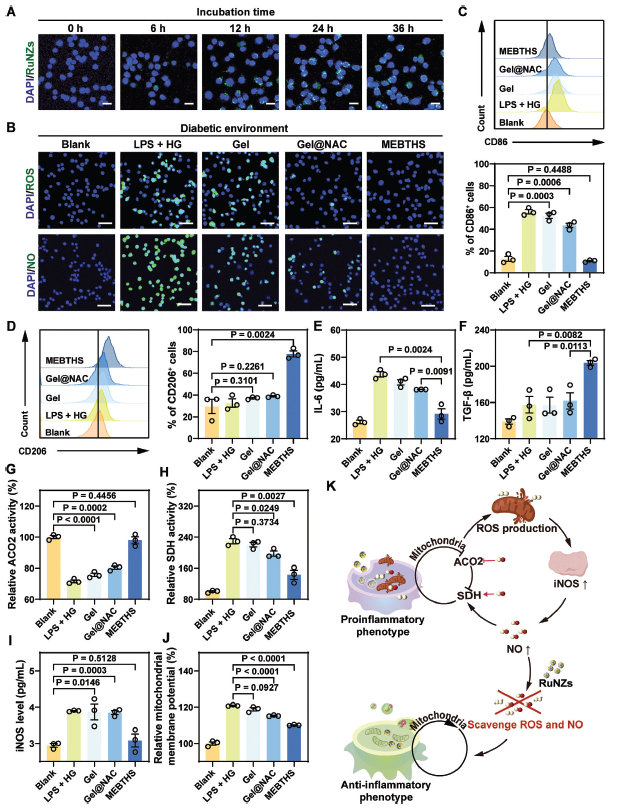
图4 MEBTHS通过清除NO和ROS来调节线粒体代谢,从而协调巨噬细胞重编程
4
MEBTHS恢复了生理性骨重塑
氧化应激和持续炎症显著损害了骨髓间充质干细胞和内皮细胞的生物学功能。具有多酶活性的MEBTHS有望保护骨髓间充质干细胞和内皮细胞免受ROS的侵害,促进巨噬细胞再极化,实现生理性骨重塑(图5A)。MEBTHS有效减轻了氧化应激诱导的BMSCs和HUVECs损伤(图5B)。MEBTHS通过巨噬细胞表型转换显著促进细胞因子的分泌,包括BMP-2和VEGF(图5C,D)。
MEBTHS处理的巨噬细胞的条件培养基培养的骨髓间充质干细胞表现出显著增强的成骨能力,细胞内碱性磷酸酶(ALP)活性显著增加(图5E,G)。MEBTHS处理巨噬细胞的条件培养基培养后,HUVECs的成管能力显著提高,形成了毛细血管样网络,结密度、总网长和分支数均增加(图5F,H)。这些发现强调了MEBTHS在创造有利的微环境方面的潜力,该微环境支持巨噬细胞、骨髓间充质干细胞和内皮细胞之间复杂的相互作用,从而使糖尿病下颌缺损恢复自我再生能力并启动生理性骨重塑过程。
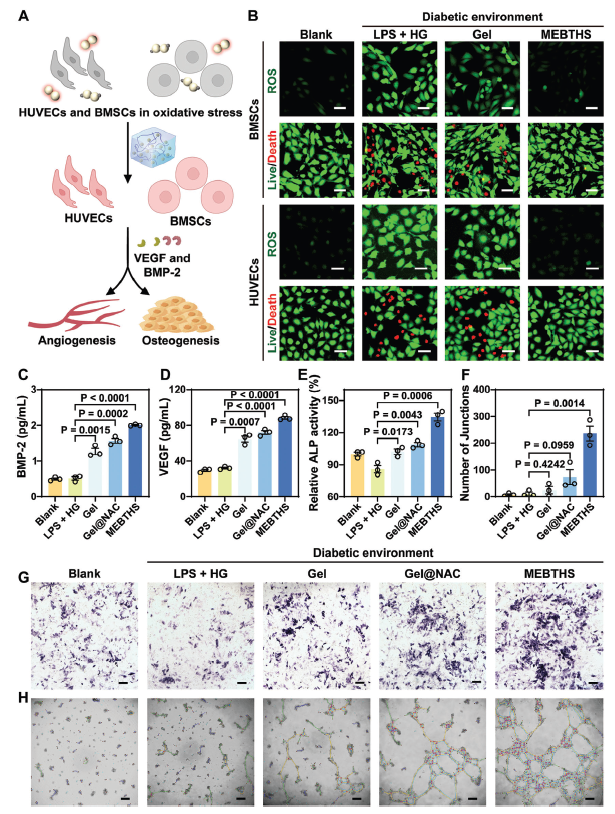
图5 MEBTHS介导体外血管生成和骨生成改善
5
MEBTHS诱导糖尿病下颌骨缺损的体内自我再生修复
利用MEBTHS的多酶活性,有效降低NO水平,从而将巨噬细胞代谢从糖酵解转向OXPHOS, iNOS表达减少,ACO2表达增加(图6A)。植入MEBTHS后,抗炎巨噬细胞明显增加,促炎巨噬细胞明显减少(图6B,C)。MEBTHS治疗的糖尿病小鼠下颌骨缺损中CD86表达的降低和CD206表达的增加进一步证实了这种转变(图6D)。这些发现证实,具有多酶活性的MEBTHS成功地协调了巨噬细胞从促炎表型向抗炎表型的重编程。
鉴于血管生成在支持膜内骨化中的重要作用,进一步研究了不同治疗方法下糖尿病下颌缺损的新生血管生成能力。MEBTHS处理的小鼠表现出强大的血管生成反应(图6E),归因于巨噬细胞复极化增强,而对照组和凝胶组显示出最小的血管形成。此外,植入后4周和8周的micro-CT分析显示,MEBTHS组的骨生长更快(图6F-H)。骨量/组织体积(BV/TV)和骨矿物质密度(BMD)进一步证实了这一观察结果。值得注意的是,MEBTHS有效地将矿化恢复到与正常小鼠相当的水平。这些发现巩固了MEBTHS恢复生理骨重塑过程的概念,使糖尿病患者的下颌骨能够自我再生修复。
为了进一步探讨MEBTHS对骨修复质量的益处,利用3D切片软件中的radiomics插件分析术后8周新形成骨的放射组学特征。分析显示,MEBTHS处理小鼠新形成的骨在表面积、强度、粗糙度和结构复杂性方面表现出优越的特征,与正常骨非常相似(图6I-L)。总之,这些共同的结果表明,MEBTHS具有多酶的性能,可以有效地调节巨噬细胞表型,促进糖尿病下颌缺损部位的成骨分化和血管生成,最终促进与正常骨质量相当的下颌骨形成(图6M)。
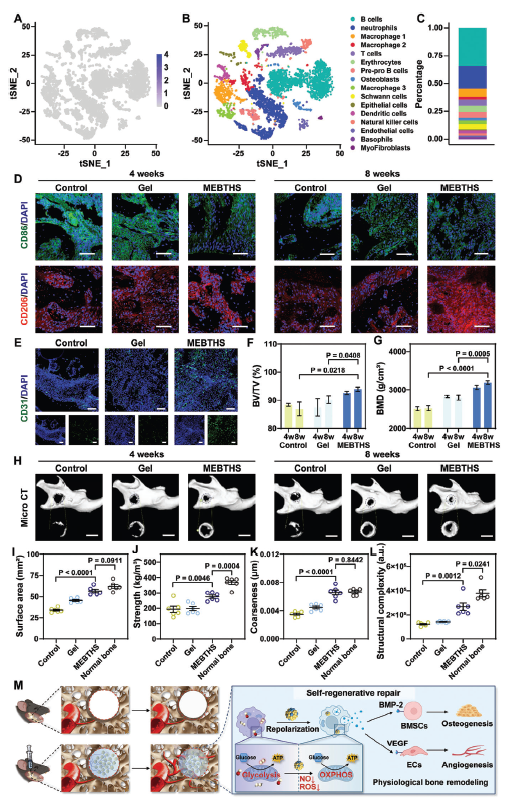
图6 MEBTHS修复糖尿病下颌骨缺损的自我再生修复
和元服务
和元生物提供多组学服务(如全外显子测序、转录组、Astral蛋白组、非靶向代谢组、非靶向脂质组、靶向代谢组、16s/ITS/18s扩增子测序、宏基因组、Cut&Tag、MeRIP (m6A)-seq、全基因组甲基化测序、简化甲基化测序等)和单细胞及空间转录组服务(如10x单细胞转录组、10x单细胞转录组及TCR/BCR、墨卓单细胞转录组、10x CytAssist空间转录组、10x HD空间转录组、Stereo-seq 空间转录组等),致力于为广大生命科学家、医学工作者提供基于多组学的科研及临床应用解决方案。