推荐产品
公司新闻/正文
基于CRISPR/Cas9系统的基因编辑策略该怎么选?
人阅读 发布时间:2023-05-09 14:13
在科学研究过程中,往往需要对细胞进行基因编辑,CRISPR/Cas9系统已经成为基因编辑的有力工具。为实现基因编辑,我们需要将CRISPR/Cas9系统组分递送至细胞内,按照递送的内容可分为以下3种:
(1)递送编码Cas9和sgRNA的质粒DNA;
(2)递送Cas9 mRNA和sgRNA;
(3)递送Cas9蛋白和sgRNA,二者可以结合形成核糖核蛋白(ribonucleoprotein, RNP)。
而递送方法则包括:物理方法(微注射、电穿孔、核感染和膜变形)、病毒载体和非病毒载体。其中,利用慢病毒转导质粒和电穿孔递送RNP是将CRISPR/Cas9导入细胞的两种主要方法(和元生物都可以提供)。
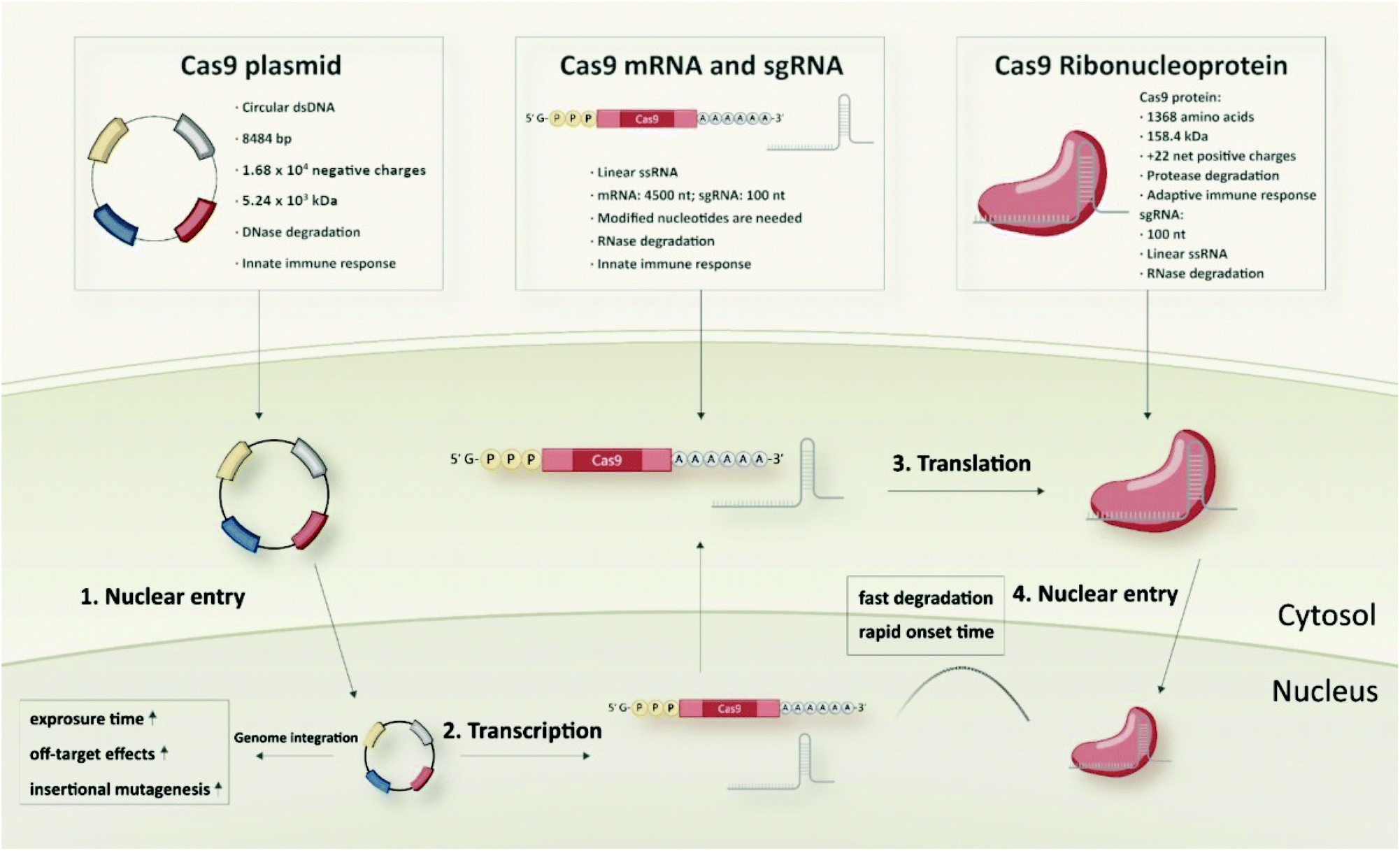
图1. CRISPR/Cas9系统的不同递送形式[1]
递送内容和方法如此多样,我们应该如何选择呢?
递送质粒是基因编辑的经典形式,它在CRISPR技术刚刚问世即被广泛使用。随着技术的发展,人们逐渐发现质粒通常不是最佳的递送形式,原因有以下几点:
1.质粒本身或者用于转染的试剂可能引起细胞毒性;
2.利用慢病毒载体时,质粒会整合到基因组DNA(即使质粒瞬转,仍有这一可能),整合位置的随机性导致对细胞的影响不可预测,另外Cas9的长时间持续表达会导致非靶向位点的编辑概率增加,放大脱靶效应,此外也可能引起免疫应答;
3.质粒进入细胞后需要入核转录,对于Cas9蛋白还需要出核翻译为蛋白,而后再入核发挥编辑功能,这一过程会使基因编辑效率降低,时效性也相对较差;
4.Cas9蛋白编码序列较长,质粒尺寸过大会增加CRISPR/Cas9系统递送和表达的难度,尤其对于本身难于转染的细胞类型,因此可应用范围受限。
因此,我们更加推荐通过电穿孔递送RNP(Cas9蛋白-sgRNA)的形式,它能有效克服上述问题,优势明显:
1、无需繁琐的分子克隆与病毒包装纯化,准备工作少;
2、毒性低,更安全;
3、不整合基因组,半衰期短,脱靶效应低;
4、Cas9蛋白与sgRNA直接发挥作用,编辑效率高、周期短;
5、对于难转染细胞(如悬浮细胞、原代细胞、干细胞等)更为理想。
此外,这种方式也有利于转染多条sgRNA进行多靶点编辑,而无需构建多靶点CRISPR载体。因此对于敲除细胞株构建,只要能够在合适位置设计出多条有效的sgRNA,和元生物会优先考虑基因前后设计2条sgRNA进行片段敲除,相比于单个位点小规模插入缺失,敲除效果更加明确(图2)。
这种方式也存在一些缺陷,它成本更高,也缺少抗性筛选的机制,但是编辑效率高可以一定程度弥补这一缺陷。

图2. 插入缺失与片段敲除对比[2]
相信大家对于如何选择合适的基因编辑方式有了一定的了解,针对敲除细胞株构建,和元生物也为大家提供慢病毒转导以及电穿孔转染RNP两种方式的选择,以满足不同的需求。利用高效的电转RNP的方法,除了基因敲除,我们还可以提供难度更高的内源点突变以及片段敲入等单克隆细胞株构建服务。综上所述,针对基于CRISPR/Cas系统的基因编辑技术,和元生物可以提供以下服务:
1、慢病毒转导质粒构建敲除单克隆细胞株
2、电穿孔转染RNP构建敲除单克隆细胞株
3、电穿孔转染RNP构建内源点突变单克隆细胞株
4、电穿孔转染RNP构建片段插入/基因融合单克隆细胞株
现在构建敲除单克隆细胞株,还有优惠活动哦,欢迎垂询!

参考文献:
[1] Lin, Y., Wagner, E., & Lächelt, U. (2022). Non-viral delivery of the CRISPR/Cas system: DNA versus RNA versus RNP. Biomaterials Science, 10(5), 1166-1192.
[2] Kapusi, E., Corcuera-Gómez, M., Melnik, S., & Stoger, E. (2017). Heritable genomic fragment deletions and small indels in the putative ENGase gene induced by CRISPR/Cas9 in barley. Frontiers in Plant Science, 8, 540.
业务咨询